Введение
Азотсодержащие вещества занимают особое место в школьном курсе химии. Они разнообразны и важны для будущих ученых, медиков и инженеров. Изучая амины, ты осваиваешь методы анализа функциональных групп, приобретаешь навыки построения структурных формул и предсказания характера реакций.
Аминокислоты, как строительные блоки белков, помогают понять работу живой клетки и происхождение белковых молекул.
При работе с аммиаком и его производными важно соблюдать технику безопасности. Эти соединения могут быть опасны при неправильном хранении, а экологические аспекты их использования также важны, так как они могут загрязнять воздух и воду.
Изучение аминов развивает научное мышление и аналитические навыки, формируя основу для дальнейшего обучения в колледже и университете.
Почему важно изучать амины
- Формирование научной картины мира: амины помогают понять биологические и химические процессы вокруг нас.
- Подготовка к будущему обучению: знание аминов необходимо для медицинских, фармацевтических и инженерных специальностей.
- Развитие интеллектуального потенциала: работа с аминами развивает аналитическое и абстрактное мышление.
- Практическая польза: аммиак и аминокислоты участвуют в создании лекарств, удобрений и материалов.
- Экологический аспект: понимание химии аминов важно для безопасного обращения с отходами.
- Выбор профессии: знания об аминах позволяют осознанно выбирать между профессиями, связанными с наукой, технологией или здравоохранением.
- Практическая ценность для здоровья: гистамин, как пример аминов, участвует в аллергических реакциях.
- Популяризация науки: чем больше молодых людей увлечено исследованием химических соединений, тем больше перспективных учёных появится в будущем.
- Технологическая подготовка: азотсодержащие соединения используются при разработке инновационных технологий.
- Общечеловеческая значимость: амины применяются в косметике, лекарствах, топливе и строительных материалах.

План изучения
- Общая характеристика класса аминов.
- Номенклатура и классификация аминов.
- Химические свойства алифатических аминов.
- Химические свойства анилина.
- Способы получения аминов.
Что такое амины
Амины — это производные аммиака NH₃, в молекуле которого атом водорода замещён углеводородным радикалом (-R).
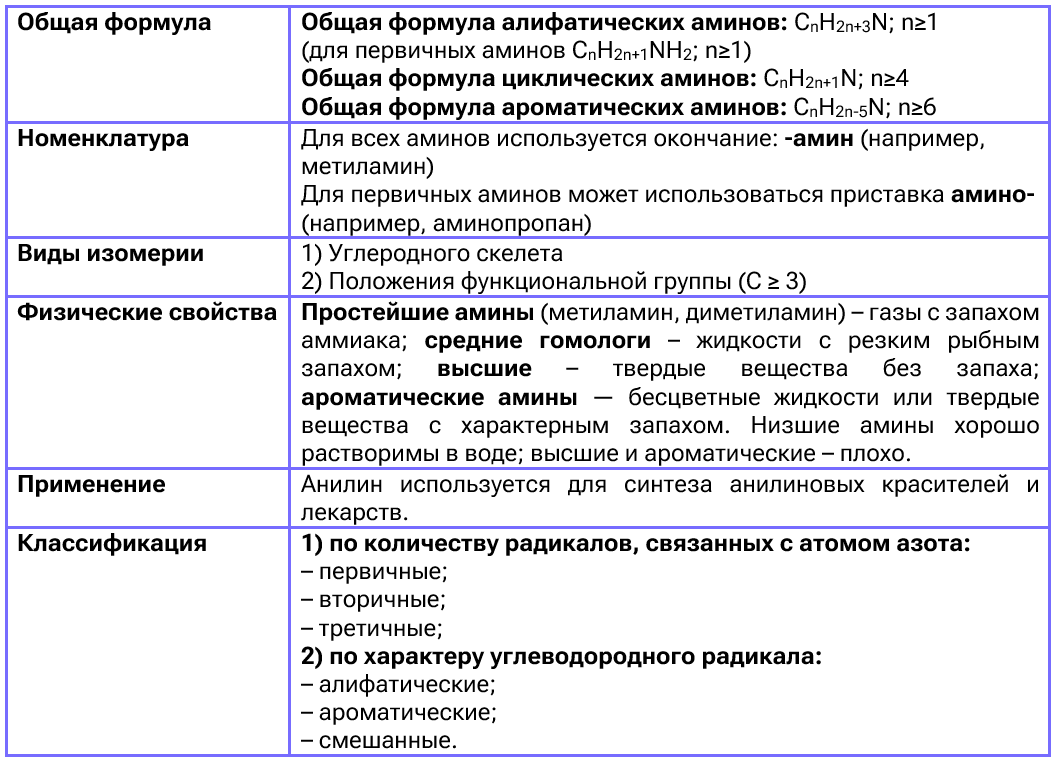
То есть амины классифицируются по количеству углеродных цепей, соединённых с атомом азота. Они подразделяются на три категории: первичные, вторичные и третичные. Например, диметиламин относится ко вторичным аминам, а триметиламин — к третичным.
Интересные факты
История изучения аминов началась ещё в XVIII веке, когда шведский химик Карл Вильгельм Шееле выделил один из простейших аминов — этиламин.
Многие природные ароматы обусловлены присутствием аминов. Например, ананасовые нотки многим продуктам придают именно амины. В то же время для ряда представителей этого класса характерен специфический «рыбный» запах, связанный с распадом белковых соединений.
Номенклатура аминов
Название первичных аминов образуется из названий углеводородных радикалов и суффикса –амин:
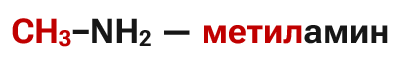
Классификация аминов
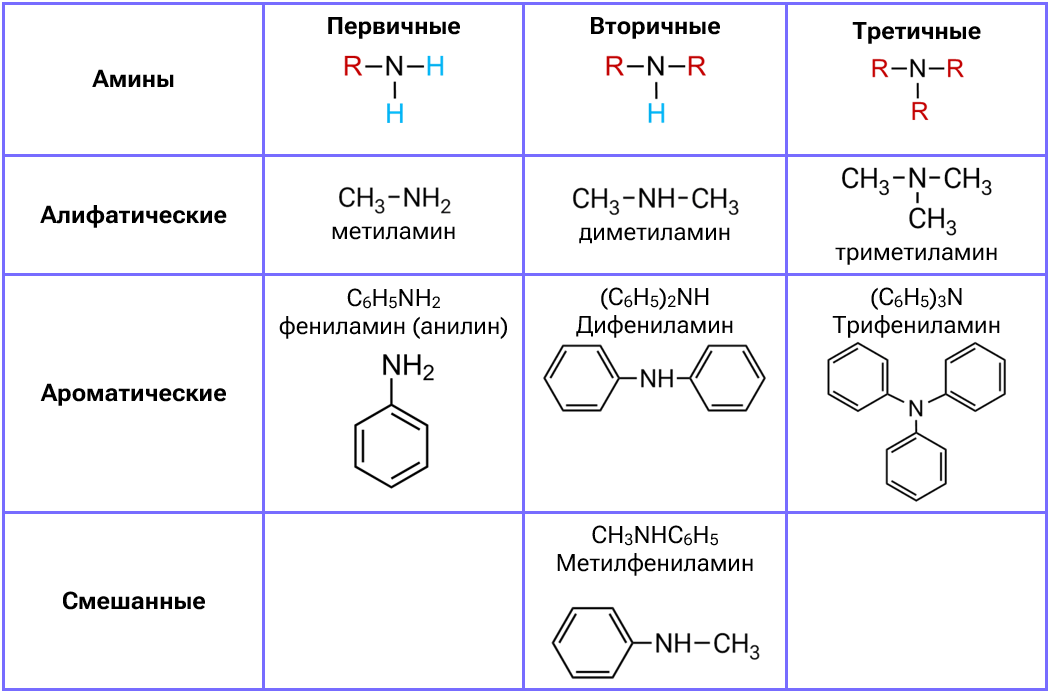
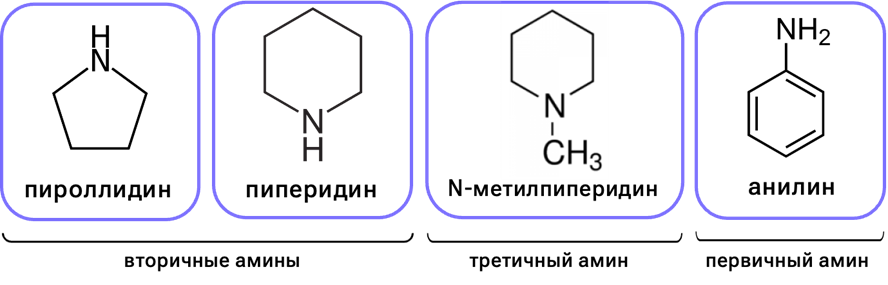
Некоторые лекарства, например, антибиотик пенициллин и обезболивающие, содержат молекулы аминов.
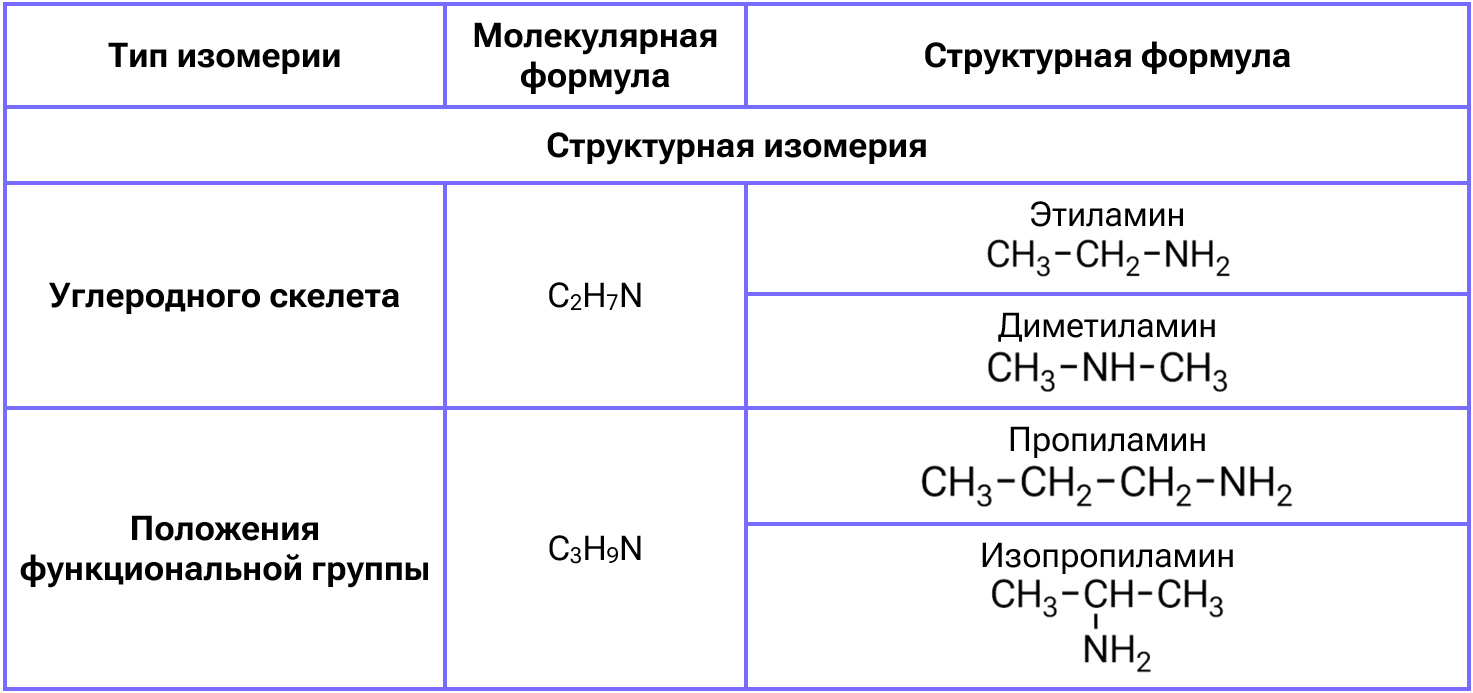
Изомерия
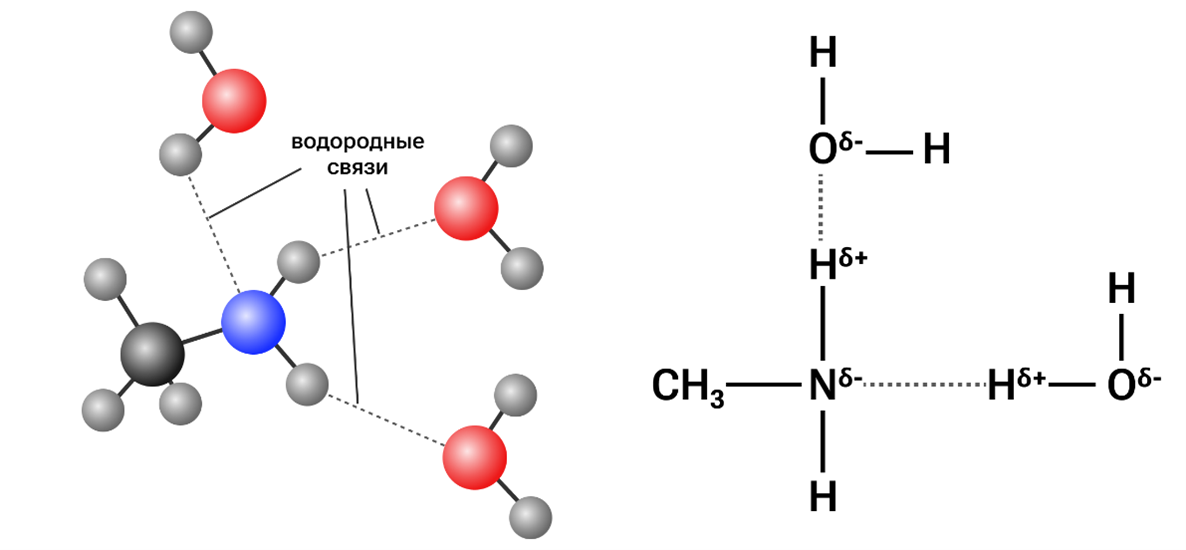
Водородная связь
Водородные связи формируются как между молекулами первичных и вторичных аминов, так и между молекулами аминов и воды. Благодаря наличию водородных связей между молекулами низкомолекулярных аминов и водой обеспечивается высокая растворимость аминов в водной среде.
С увеличением числа и размеров углеводородных заместителей растворимость аминов в воде уменьшается. Это связано с возрастанием стерических препятствий, которые мешают формированию водородных связей. Ароматические амины практически нерастворимы в воде.
Особенности строения аминов
Аминогруппа имеет центральный атом азота с sp³-гибридизацией, поэтому связи в пространстве образуют тетраэдр.
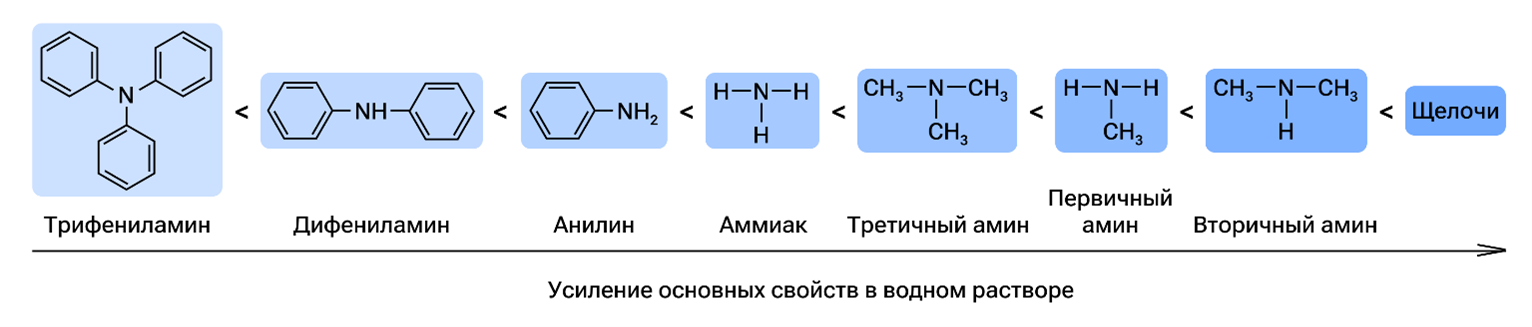
Основность аминов обусловлена присутствием свободной электронной пары у атома азота, которая способствует образованию координационной связи посредством механизма донор-акцепторного взаимодействия.
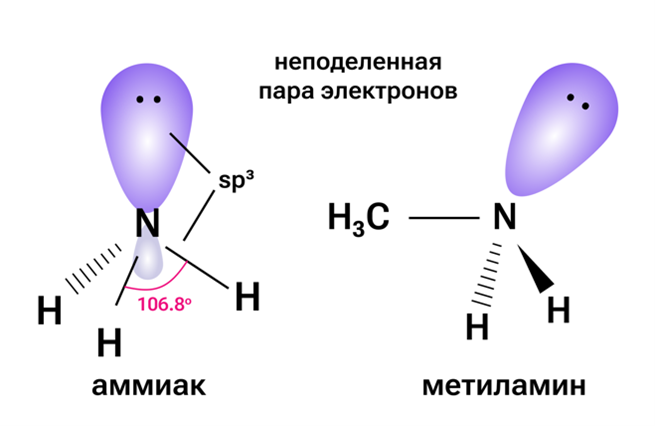
Основные характеристики насыщенных алифатических аминов проявляются интенсивнее, чем у аммиака, поскольку алкильные группы типа −СН₃, −С₂Н₅ и прочие повышают электронную плотность около атома азота.
Химические свойства аминов
Строение аминов аналогично строению аммиака, поэтому они демонстрируют сходные химические свойства. Помимо общих характеристик, ароматическим аминам присущи реакции замещения непосредственно в бензольном цикле.
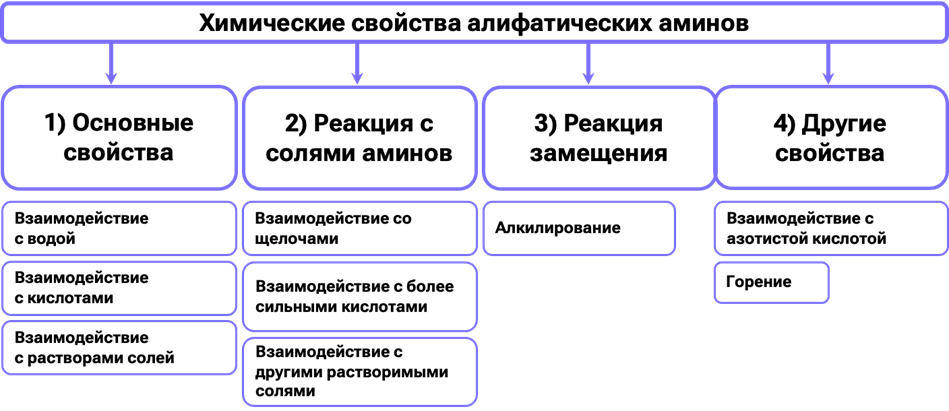
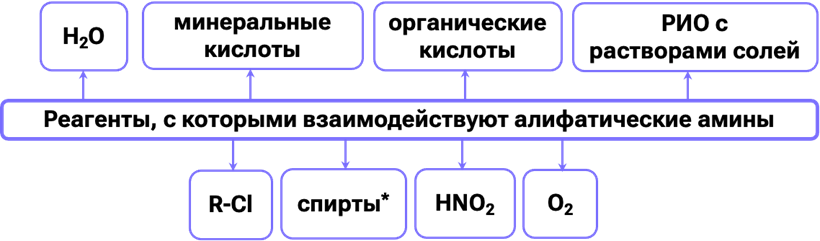
Теперь подробно рассмотрим химические свойства аминов.
1. Основные свойства
1. Взаимодействие аминов с водой
Все амины характеризуются наличием основных свойств, поскольку представляют собой производные аммиака и вступают в реакцию с водой, образуя соответствующие гидроксиды.
Взаимодействие аммиака с водой:

Эта реакция демонстрирует равновесие, которое возникает при контакте газообразного аммиака с жидкой водой. Молекула аммиака принимает протон (H⁺) от воды, становясь положительным ионом аммония (NH₄⁺), в то время как молекула воды теряет протон, превращаясь в отрицательный ион гидроксида (OH⁻). Реакция иллюстрирует свойство аммиака проявлять основные свойства, действуя как акцептор протонов, и подтверждает факт образования слабощелочного раствора аммиачной воды.
Взаимодействие метиламина с водой:

Этот процесс подчёркивает высокую нуклеофильность метиламина и объясняет его способность вызывать повышение рН при растворении в воде.
Заметка: в водных растворах алифатические амины проявляют себя как слабые электролиты, то есть слабые основания, имеющие щелочную среду.
Алифатические амины значительно сильнее аммиака, тогда как ароматические амины заметно уступают последнему. Причина кроется в способности алкильных групп повышать электронную плотность возле атома азота.
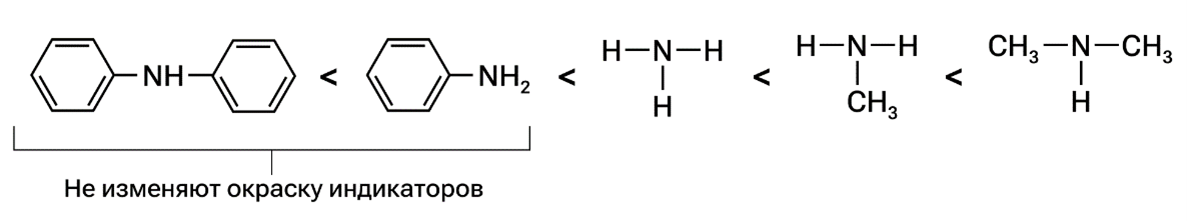
Цветовые изменения индикаторов зависят от природы аминов: алифатические амины вызывают переход цвета лакмуса в синий оттенок, метилоранжа — в жёлтый, а фенолфталеина — в ярко-малиновый.
Важно, что присутствие фенильного радикала существенно ослабляет электронодонорные свойства атома азота, делая анилин настолько слабым основанием, что оно не вступает в химическое взаимодействие с водой и не меняет окраску индикаторов. Подобное поведение характерно и для прочих представителей ароматической группы аминов.
2. Особенности взаимодействия аминов с кислотами
Амины способны реагировать с кислотами с образованием устойчивых солей. Такие соли обычно представляют собой твёрдые вещества без выраженного запаха, хорошо растворимые в воде и практически нерастворимые в органических растворителях.
Взаимодействие аммиака с соляной кислотой:

Реакция востребована в сельскохозяйственном секторе, она образует хлорид аммония — важное удобрение, обогащающее почву азотом.
Реакция аммиака с соляной кислотой иллюстрирует классический пример проявления свойств оснований и кислот по Бренстеду-Лоури.
Заметка: теория Бренстеда-Лоури, предложенная независимо датским химиком Йоханнесом Бренстедом и английским учёным Томасом Лоури в 1923 году, стала фундаментальным вкладом в развитие современной химии.
Согласно этой теории, кислота определяется как вещество, способное отдавать протоны (протоны водорода), тогда как основание — это молекула или ион, способные присоединять протоны. Каждая кислота должна иметь сопряжённое основание, а каждое основание — сопряжённую кислоту. Этот принцип называется принципом сопряжения кислот и оснований.
Теория Бренстеда-Лоури помогает объяснить поведение растворов электролитов, механизмы реакций кислотно-щелочного титрования, природу катализаторов и многие другие процессы. Например, кислотно-основные индикаторы меняют свою окраску именно потому, что реагируют с растворами кислот и оснований, меняя свое состояние в зависимости от концентрации протонов.
У теории Бренстеда-Лоури есть ограничения. Она неприменима к веществам, не содержащим водорода, таким как оксиды металлов, ионам фтора и другим анионам, которые действуют как основания, хотя и не принимают протоны. Для объяснения поведения таких веществ была разработана более общая теория Льюиса, которая рассматривает кислоты и основания с точки зрения акцептирования и донорства электронных пар.
Взаимодействие этиламина с соляной кислотой:
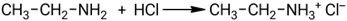
Взаимодействие метиламина с бензойной кислотой:

Взаимодействие избытка метиламина с щавелевой кислотой:
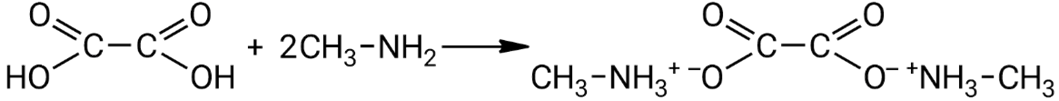
Поскольку в реакции избыток метиламина, оба протона щавелевой кислоты участвуют в образовании двух ионов метиламмония. Эта реакция демонстрирует, как происходит взаимодействие основания (метиламина) с многоосновной кислотой (щавелевой кислотой), приводящее к образованию соответствующей соли.
Взаимодействие циклогексиламина с бромоводородной кислотой:
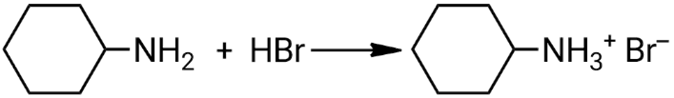
Взаимодействие 1,4-диаминоциклогексана с избытком иодоводородной кислоты:
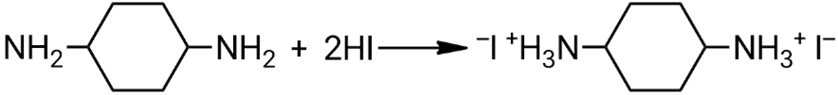
Взаимодействие метиламина с недостатком серной кислоты:
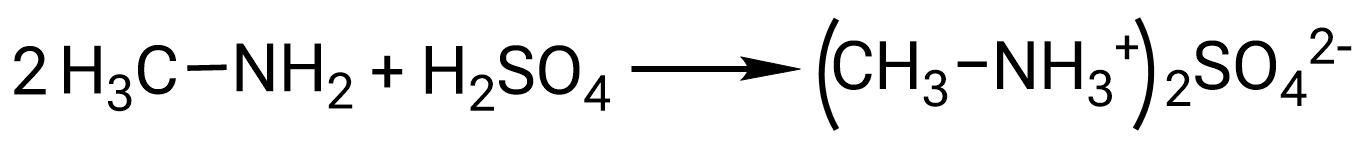
Взаимодействие метиламина с избытком серной кислоты:

Взаимодействие раствора этиламина с избытком CO₂:
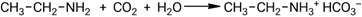
Эта реакция важна для понимания принципов поведения аминов в кислых средах и роли, которую выполняют амины в механизмах стабилизации уровня кислотности жидкостей, например, в биологических системах.
Взаимодействие диэтиламина с уксусной кислотой:

Взаимодействие N-метилпиперидина с соляной кислотой:
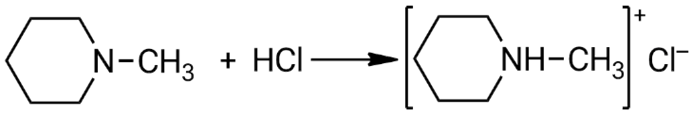
N-метилпиперидин — азотсодержащий гетероцикл, то есть органическое соединение, в цикле которого вместе с углеродом присутствует атом азота. Это производное пиперидина с шестичленным циклом, в котором атом азота связан с метильной группой. Такая структура делает молекулу высокореакционной: она легко вступает в реакции алкилирования, нитрования, сульфирования и другие процессы модификации.
N-метилпиперидин широко используется в синтезе лекарственных препаратов и биологически активных соединений. Его структура позволяет создавать функциональные группы с различными фармакологическими свойствами. Например, производные N-метилпиперидина применяются как анальгетики, антидепрессанты и противосудорожные средства, в том числе известный антигистаминный препарат димедрол.
Кроме фармацевтики, соединение используется в сельском хозяйстве (гербициды, фунгициды) и в косметологии и парфюмерии, где улучшает свойства продуктов и ароматических композиций.
Получают N-метилпиперидин различными методами, включая каталитический гидрогенез пиперонилина и аммонолиз предшественников. Для контроля качества и идентификации применяются хроматография и масс-спектрометрия.
Таким образом, N-метилпиперидин и другие азотсодержащие гетероциклы являются важными строительными блоками современной химии и медицины. Их уникальные химические и физические свойства делают их незаменимыми для разработки новых лекарств, агрохимикатов и специализированных материалов. Дальнейшие исследования открывают перспективы для новых синтезов и применения этих соединений.
Взаимодействие анилина с соляной кислотой:
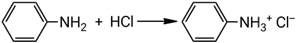
Заметка: ароматические амины вступают в реакции исключительно с сильными кислотами.
3. Взаимодействие алифатических аминов с растворимыми солями
Алифатические амины могут взаимодействовать с растворимыми солями с образованием нерастворимых гидроксидов.
Взаимодействие аммиака с раствором хлорида железа(II):

Взаимодействие этиламина с раствором хлорида железа(II):
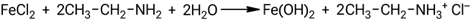
Заметка: взаимодействие алифатических аминов с растворами солей является реакцией ионного обмена.
2. Свойства солей аминов
1. Взаимодействие солей аминов со щелочами
Соли аминов могут взаимодействовать со щелочами. Реакции сопровождаются выделением газа.
Взаимодействие хлорида аммония с гидроксидом калия:
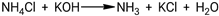
Выделяется газообразный аммиак с характерным запахом, что можно применять в лабораторных условиях.
Взаимодействие хлорида метиламмония с гидроксидом калия: {{«isPartOf»: { «@type»: «Book», «name»: «Репетитор по химии (под редакцией А. С. Егорова)»} }}

Взаимодействие ацетата этиламмония с гидроксидом кальция:
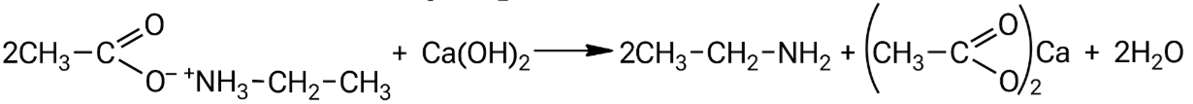
Эта реакция известна как качественная проба на определение аминов: выделяющийся этиламин легко обнаружить по резкому запаху, подобному аммиаку.
Взаимодействие формиата диметиламмония с гидроксидом натрия:

Важно: взаимодействие солей аминов со щелочами при нагревании — это качественная реакция на соли аминов.
2. Взаимодействие солей аминов с другими солями
Соли аминов способны взаимодействовать с другими растворимыми солями.
Взаимодействие хлорида аммония с нитратом серебра:
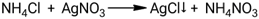
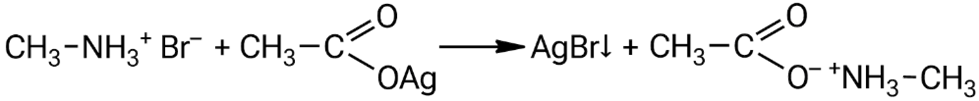
Взаимодействие бромида метиламмония с ацетатом серебра:
Взаимодействие сульфата этиламмония с хлоридом бария:
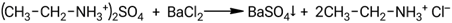
Взаимодействие гидросульфата этиламмония с хлоридом бария:
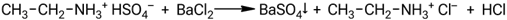
Заметка: реакции ионного обмена между солями аминов и другими растворимыми солями протекают только в том случае, если выпадает осадок.
3. Взаимодействие солей аминов слабых кислот с растворами более сильных кислот
Соли аминов, содержащие в качестве кислотного остатка анионы слабых кислот, способны реагировать с растворами более сильных кислот.
Взаимодействие ацетата метиламмония с соляной кислотой:
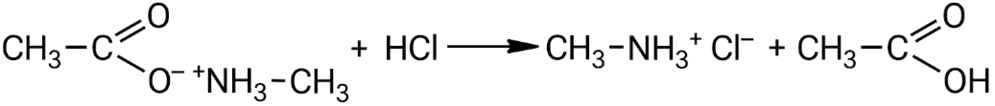
Взаимодействие гидрокарбоната этиламмония с избытком серной кислоты:
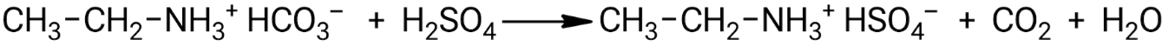
3. Реакции замещения
1. Алкилирование
Реакция аммиака или аминов с галогеналканами при нагревании приводит к их последовательному алкилированию. При этом из аммиака образуются соли первичных аминов, из первичных аминов — соли вторичных аминов, из вторичных аминов — соли третичных аминов.
Взаимодействие аммиака с бромметаном:

Взаимодействие метиламина с бромметаном:

Взаимодействие диметиламина с бромметаном:
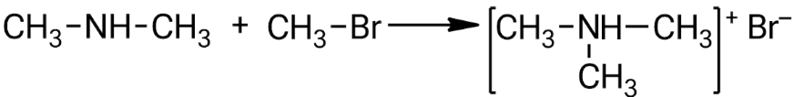
Взаимодействие триметиламина с бромметаном:
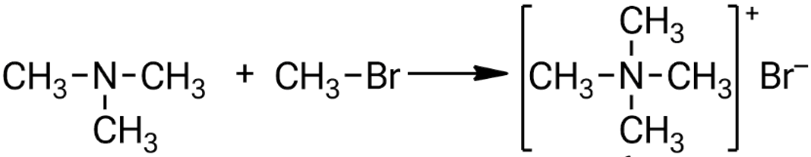
Взаимодействие пирролидина с хлорэтаном:
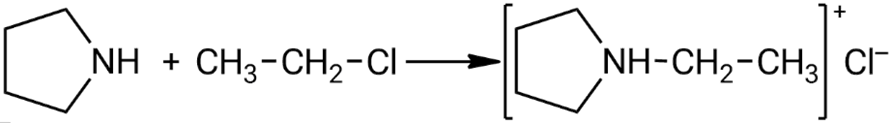
Взаимодействие анилина с хлорметаном:

Заметка: при алкилировании аммиака и аминов галогеналканами на первой стадии образуются соли, поэтому для получения аминов полученные соли необходимо обработать раствором щёлочи.
Другим возможным способом алкилирования является взаимодействие аммиака и аминов со спиртами при нагревании в присутствии оксида алюминия.
Взаимодействие аммиака с этанолом:
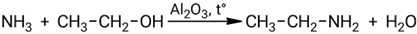
Этот процесс важен в органическом синтезе, поскольку демонстрирует простой путь получения аминов из простых исходных веществ — аммиака и спиртов. Реакция обратима и может проходить в присутствии подходящего катализатора, облегчающего удаление воды и сдвигая равновесие вправо.
Взаимодействие метиламина с этанолом:
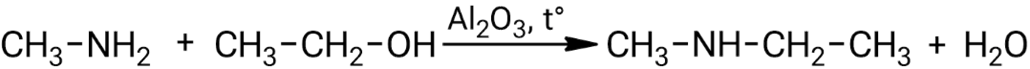
4. Другие важные свойства аминов
1. Реакции алифатических аминов с азотистой кислотой
Первичные алифатические амины при взаимодействии c HNO₂ образуют первичные спирты и молекулярный азот.

Взаимодействие метиламина с азотистой кислотой:
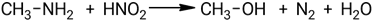
Взаимодействие изопропиламина с азотистой кислотой:

Взаимодействие 1,3-диаминопропана с избытком азотистой кислоты:
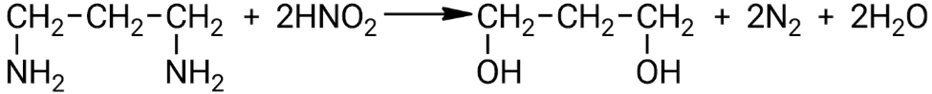
Вторичные алифатические амины, взаимодействуя с азотистой кислотой (HNO₂), преобразуются в нитрозоамины с общей формулой R₂N−N=O, представляющие собой маслянистые жидкости жёлтой окраски, отличающиеся специфичным ароматом.
Заметка: задачи на реакции вторичных аминов с азотистой кислотой в ЕГЭ по химии не встречаются.
Взаимодействие диметиламина с азотистой кислотой:

Третичные алифатические амины с HNO₂ не реагируют.
2. Горение
Процесс горения аминов сопровождается выделением углекислого газа, молекулярного азота и паров воды.
Реакция горения метиламина:
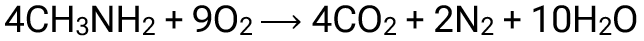
Самый важный амин: почему адреналин заслуживает особого внимания
Среди множества аминов есть один, который заслуживает отдельного рассмотрения — адреналин. Его название знакомо почти каждому: этот гормон ассоциируется со стрессом, страхом и экстренными ситуациями. Но что делает адреналин действительно особенным? Давайте разберёмся.
Биохимия адреналина
Адреналин (эпинефрин) синтезируется в основном в надпочечниках. По химической природе он относится к катехоламинам — группе аминов, содержащих две важные функциональные группы: аминогруппу (-NH₂) и гидроксил (-OH). Такая структура позволяет адреналину быстро проникать через клеточные мембраны и влиять на разные органы и системы организма.
Физиология адреналина
При стрессе, испуге или опасности организм выбрасывает адреналин, запускающий каскад реакций, известный как реакция «бей или беги». Основные эффекты:
- Повышение артериального давления и учащение сердцебиения.
- Расширение зрачков для улучшения зрения.
- Ускорение дыхания, чтобы увеличить поступление кислорода.
- Перераспределение крови от внутренних органов к мышцам, обеспечивая готовность к действию.
Эти механизмы позволяют организму мгновенно адаптироваться к экстремальным ситуациям, повышая шансы на выживание.
Медицинские применения
Адреналин активно используется в медицине. Особенно важно его применение в случаях аллергических реакций (анафилактического шока), остановке сердца и приступах астмы. Адреналин способен спасти жизнь, возвращая сердце к нормальной работе и восстанавливая дыхание пациента.
Уникальность среди аминов
Адреналин считается одним из важнейших аминов, потому что играет двойную роль: он одновременно действует как гормон и как нейромедиатор, влияя на множество процессов в организме.
Анилин: от биологических к органическим аминам
Хотя адреналин — это биологически активный амин, влияющий на физиологические процессы, в химии аминов также изучают их свойства на примере простых органических соединений. Одним из таких важных представителей ароматических аминов является анилин.
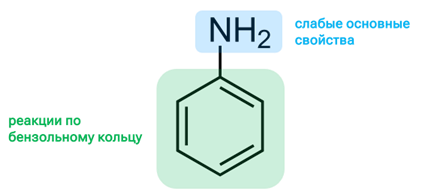
Химические свойства анилина
Ароматические амины, в том числе и анилин, вступают в реакции замещения по бензольному кольцу. Аминогруппа — заместитель I рода, направляет замещение в орто- и пара-положения. Реакции замещения происходят гораздо легче, чем в случае аренов.
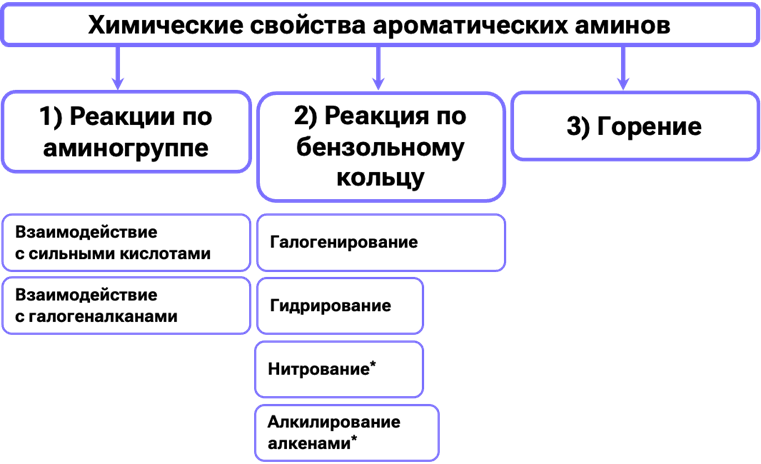
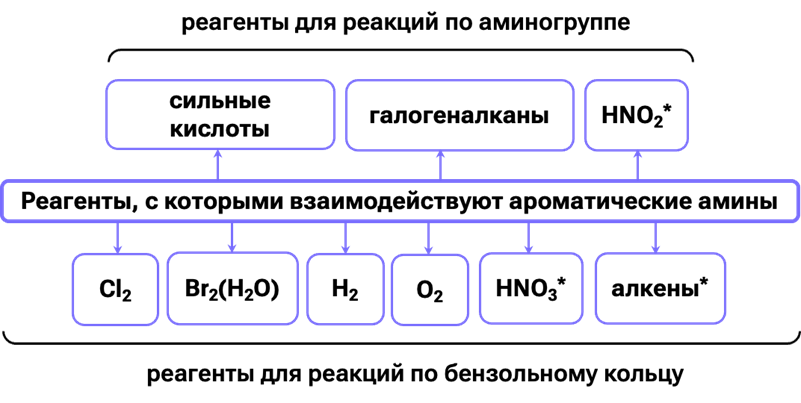
Реакции по бензольному кольцу
1. Галогенирование
Анилин вступает в реакции с хлором и бромной водой. Наличие аминогруппы определяет его принадлежность к заместителям I рода, обеспечивающим ориентацию замещающих групп преимущественно в орто- и пара-положениях бензольного кольца. Такие реакции протекают значительно активнее, чем аналогичные процессы с участием чистого бензола.
Взаимодействие анилина с хлором:
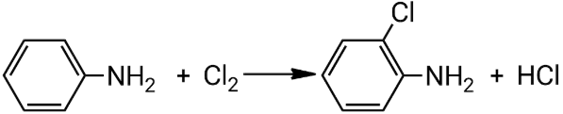
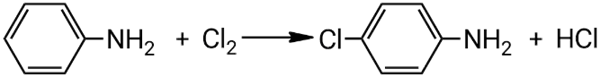
При хлорировании получается смесь орто- и пара-хлоранилина.
Взаимодействие анилина с бромной водой:
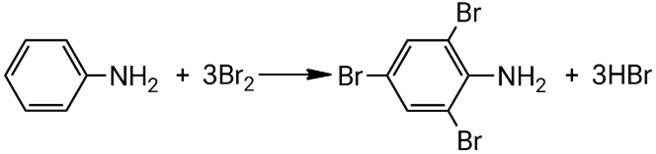
Взаимодействие 2-метиланилина с бромной водой:
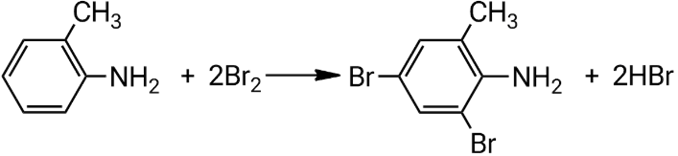
Взаимодействие 3-метиланилина с бромной водой:
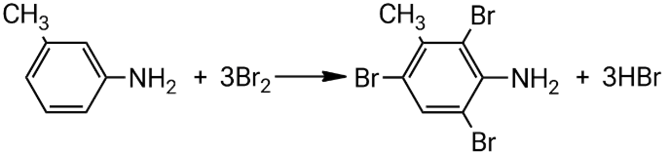
Взаимодействие 4-метиланилина с бромной водой:
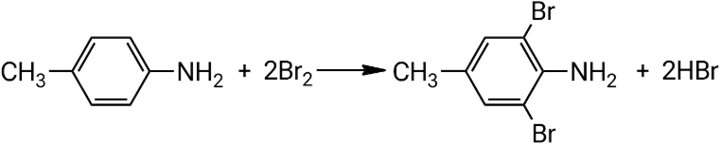
Заметка: обесцвечивание раствора бромной воды и образование белого осадка триброманилина (2,4,6-триброманилина) служат качественным признаком присутствия анилина и прочих ароматических аминов.
2. Гидрирование
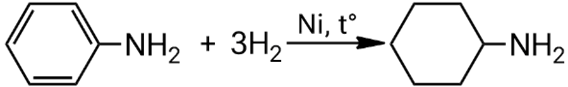
Гидрирование анилина проводят на платиновом или никелевом катализаторе при нагревании. При этом образуется циклический амин — циклогексиламин.
Гидрирование анилина:
Канцерогенные свойства анилина
Понятие канцерогенности
Канцероген — это вещество или фактор внешней среды, способствующий развитию злокачественных опухолей. Механизмы действия различны: одни вещества повреждают ДНК, вызывая мутации, другие стимулируют деление клеток или подавляют иммунитет. Обычно канцерогенное воздействие развивается постепенно и проявляется спустя годы после контакта с веществом.
Особенности анилина
Анилин получил широкую известность благодаря своим токсическим свойствам. Несмотря на полезность в промышленности (производстве красителей, пластиков, резин и лекарств), он признан опасным веществом с доказанными канцерогенными эффектами.
- Исторически были зарегистрированы случаи лейкемии среди работников красильных фабрик.
- Длительный контакт с анилином связан с повышенным риском рака мочевого пузыря, желудка и печени.
- Метаболизм анилина в организме приводит к образованию N-гидроксианилинов и N-ацетилированных форм, которые взаимодействуют с ДНК, вызывая повреждения и мутации.
- Анилин также снижает активность лимфоцитов и макрофагов, ослабляя иммунный ответ против раковых клеток.
Законодательные меры защиты
Во многих странах введены строгие ограничения на использование анилина. В России установлены предельно допустимые концентрации (ПДК) для воды, пищи и воздуха на рабочих местах. Несмотря на это, контакт с анилином возможен в химической промышленности, полиграфии и на шинных заводах.
Вывод
Анилин — пример опасного канцерогена, требующего строгого контроля и мер индивидуальной защиты. Современные технологии и контроль качества снижают риски, но опасность сохраняется, подчёркивая значимость промышленной гигиены.
А что будет на ЕГЭ?
В экзаменационной программе по химии задания по аминам охватывают разные аспекты и требуют комплексного понимания темы.
Задания первой группы проверяют знание номенклатуры и классификации аминов. Нужно уметь различать первичные, вторичные и третичные амины, определять степень замещённости атома азота и правильно называть соединения по правилам IUPAC.
Тебе могут предложить построить структурные формулы аминов исходя из заданных условий. Часто задают вопросы, связанные с возможностью существования изомеров и их количеством.
Некоторые задания направлены на распознавание аминов экспериментально. Нужно знать характерные качественные реакции, которые позволяют отличить амины друг от друга и определить их наличие в смеси.
Отдельные задания посвящены применению аминов в реальной жизни. Нужно приводить конкретные примеры использования аминов в производстве лекарств, синтетических тканей, красителей и моющих средств.
Таким образом, задания ЕГЭ по теме «Амины» проверяют как теорию, так и практические навыки. Чтобы успешно справиться с ними, важно уверенно владеть номенклатурой, свойствами и реакционной способностью аминов.
Способы получения аминов
1. Промышленные способы
1. Восстановление нитропроизводных водородом
Гидрирование нитропроизводных проводят на платиновом или никелевом катализаторе при нагревании. При этом образуется предельный амин.
Взаимодействие этана с азотной кислотой:
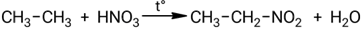
Взаимодействие нитроэтана с водородом:
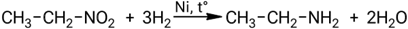
Взаимодействие динитропропана с избытком водорода:
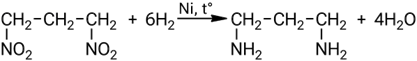
Взаимодействие бензола с нитрующей смесью:
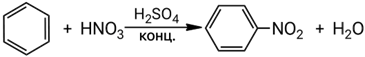
Взаимодействие нитробензола с водородом:
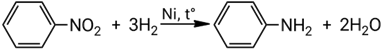
Важно: восстановление нитропроизводных — способ получения только первичных аминов.
2. Алкилирование аммиака спиртами
Одним из важных способов получения аминов является взаимодействие аммиака со спиртами при нагревании в присутствии оксида алюминия.
Взаимодействие этанола с аммиаком:
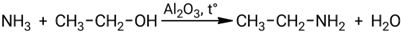
Этот процесс важен в органическом синтезе, поскольку демонстрирует простой путь получения аминов из недорогих исходных веществ — аммиака и спиртов. Реакция обратима и может проходить в присутствии подходящего катализатора, облегчающего удаление воды и сдвигая равновесие вправо. Таким образом аммиак, служащий источником аминогруппы, взаимодействует со спиртами, образуя амины.
2. Лабораторные способы
1. Восстановление нитросоединений водородом в момент выделения
Амины можно получать путём восстановления нитросоединений водородом, выделяющимся при реакции металла с кислотой. В результате образуются соли предельных аминов. Для получения аминов полученные соли нужно обработать щёлочью.
Схема реакции:
R-NO₂ + 3Fe + 7HCl ⟶ R-NH₃Cl + 3FeCl₂ + 2H₂O
Классический процесс восстановления нитросоединений до соответствующих аминов. Солянокислая среда поддерживает активную реакцию восстановления, предотвращая окисление металла и помогая поддерживать кислую среду, благоприятствующую восстановлению нитрогруппы.
Взаимодействие нитроэтана с железом в присутствии соляной кислоты:
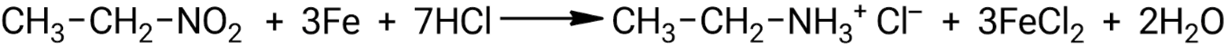
Взаимодействие нитробензола с железом в присутствии соляной кислоты:

Взаимодействие 1,3-динитробензола с цинком в присутствии соляной кислоты:
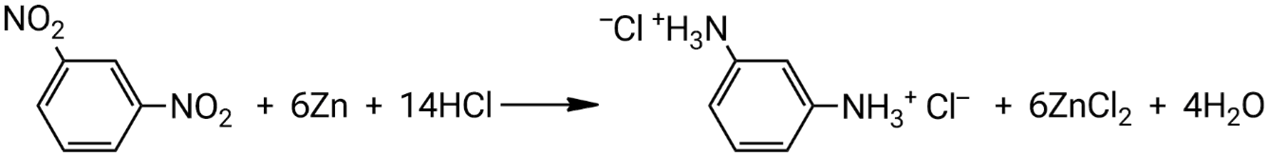
Взаимодействие 3-нитробензойной кислоты с железом с бромоводородной кислотой:
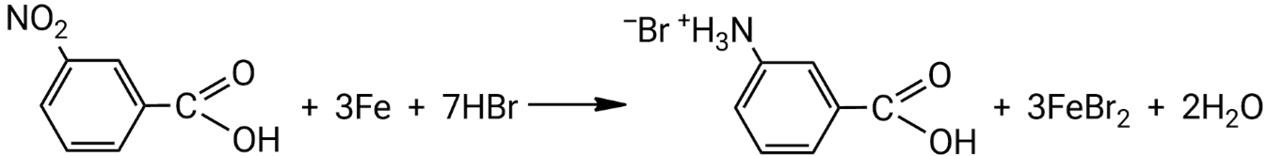
Заметка: при восстановлении нитропроизводных в кислой среде образуются соли первичных аминов.
Также амины можно получать путём восстановления нитросоединений водородом, образующимся при реакции амфотерного металла со щелочами.
Схема реакции:
R-NO₂ + 2Al + 2KOH + 4H₂O ⟶ R-NH₂ + 2K[Al(OH)₄]
Взаимодействие нитроэтана с алюминием в присутствии гидроксида калия:
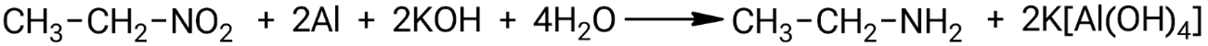
3. Взаимодействие нитробензола с сульфидом аммония
Взаимодействие нитробензола с сульфидом аммония называется реакцией Зинина и является способом получения анилина.

Поскольку нитробензол достаточно стойкое соединение, такая реакция возможна только в специальных условиях, чаще всего при нагревании и повышенной концентрации реагентов. Сера, выпавшая в осадок, сигнализирует о завершении реакции восстановления.
Заметка: задания по этой реакции в ЕГЭ не встречаются.
4. Алкилирование аммиака и аминов галогеналканами
Нагревание аммиака и аминов с галогеналканами приводит к их последовательному алкилированию. При этом из аммиака образуются соли первичных аминов, из первичных аминов — соли вторичных аминов, из вторичных аминов — соли третичных аминов.
Заметка: при алкилировании аммиака и аминов галогеналканами на первой стадии образуются соли, поэтому для получения аминов полученные соли нужно обработать раствором щёлочи.
Взаимодействие хлорэтана с аммиаком:

Хороший пример эффективного использования нуклеофильного замещения для получения ценных органических соединений.
Взаимодействие 1,3-дибромпропана с избытком аммиака:

Взаимодействие хлорбензола с аммиаком:
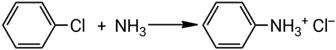
Механизм реакции: аммиак, выступающий в роли нуклеофила, атакует ароматическое кольцо, замещая атом хлора на аминогруппу. Таким образом, рассмотренная реакция демонстрирует эффективное введение аминогруппы в ароматическое ядро.
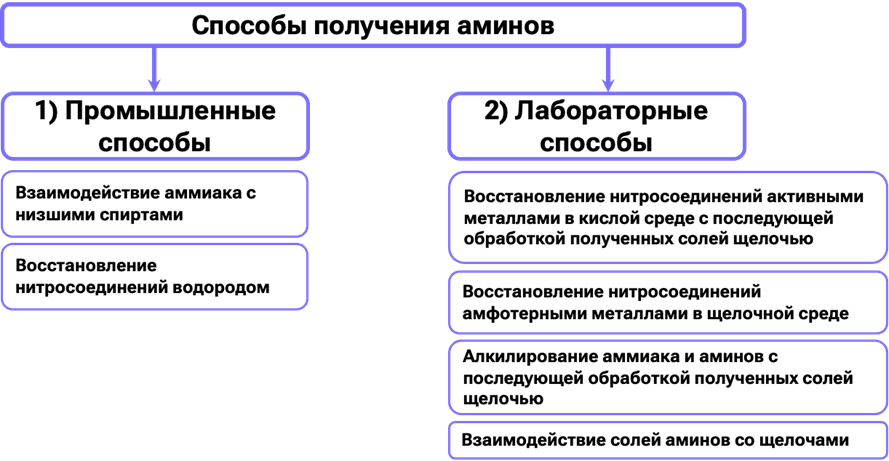
Итоговая таблица по способам получения аминов
Производство анилина в промышленных масштабах
Анилин — ключевой продукт химической промышленности, используемый в производстве красителей, медикаментов, гербицидов и полимеров.
Методы получения анилина
1. Восстановление нитробензола
Этот способ — наиболее распространённый и эффективный метод синтеза анилина. Процесс осуществляется несколькими способами:
- Каталитическое гидрирование: нитробензол обрабатывается водородом в присутствии катализатора (например, никеля Ренея).
- Электрохимическое восстановление: электролиз раствора нитробензола в кислой среде.
- Реакция Буво-Блана: гидрогенолиз нитробензола с использованием металлического натрия и спирта.
Преимущества метода:
- Высокая селективность и производительность.
- Возможность управления процессом путём подбора оптимальных условий.
Недостатки:
- Требуется значительное потребление водорода.
- Необходимость строгого контроля температуры и давления.
2. Дегидрохлорирование хлорбензолов
Метод основан на обработке хлорбензола спиртом в присутствии оснований, в результате чего образуется анилин и хлороводород.
Преимущества метода:
- Простота технологического исполнения.
- Отсутствие потребности в дорогостоящих восстановительных средствах.
Недостатки:
- Образование побочных продуктов (хлорида аммония).
- Ограниченная доступность исходного сырья.
Роль анилина в промышленности
Полученный анилин находит широкое применение:
- в производстве анилиновых красителей,
- как промежуточный продукт для синтеза лекарственных препаратов,
- в качестве компонента пластификаторов и стабилизаторов полимеров,
- в агрохимии для изготовления фунгицидов и инсектицидов.
Проблемы и перспективы развития
Несмотря на значительные успехи в области производства анилина, перед отраслью стоят важные задачи:
- Оптимизация технологических процессов для снижения энергозатрат.
- Совершенствование методов переработки отходов и уменьшение воздействия на окружающую среду.
- Исследование альтернативных путей синтеза анилина из возобновляемых источников сырья.
Таким образом, получение анилина остаётся актуальной задачей современной химической промышленности, требующей постоянного совершенствования технологий и внедрения инновационных решений.
Амины и биохимия
В биологических системах аминокислоты превращаются в амины, которые играют ключевую роль в обмене веществ. Изучение аминов помогает понять химические и биологические процессы, а также оценить их значимость в повседневной жизни и технологиях будущего.
Проверь себя
Ответь на десять вопросов и узнай, насколько хорошо удалось усвоить материал.
1. Какой класс соединений называют аминами?
A) Органические вещества, содержащие амидный фрагмент
B) Соединения с карбоксильной функциональной группой
C) Продукты замещения атомов водорода в аммиаке на углеводородные остатки
D) Углеводороды с двойной связью
C
2. Какие виды аминов существуют в зависимости от степени замещения атома азота?
A) Первичный, вторичный, четвертичный
B) Вторичный, третичный, четвертичный
C) Только первичный и вторичный
D) Первичный, вторичный, третичный
D
3. Что такое анилин?
A) Этиламин
B) Диэтиламин
C) Фениламин
D) Пропиламин
C
4. Выбери верное утверждение относительно физических свойств аминов:
A) Низшие амины обладают неприятным запахом рыбы
B) Высшие амины прекрасно растворяются в воде
C) Все амины растворимы в органических растворителях
D) Все амины кипят при температуре ниже нуля градусов Цельсия
A
5. Что происходит при взаимодействии аминов с минеральными кислотами?
A) Образуются эфиры
B) Образуются аммонийные соли
C) Происходит гидролиз
D) Ничего не происходит
B
6. Как называются соединения, в которых атом азота связан с двумя углеводородными остатками?
A) Третичные амины
B) Четвертичные амины
C) Вторичные амины
D) Первичные амины
C
7. Какой процесс называют алкилированием аминов?
A) Замещение водорода в группе -NH₂ на алкильный радикал
B) Присоединение водорода к аминному азоту
C) Окисление аминов кислородом воздуха
D) Гидролиз аминов
A
8. Какой амин является основой для большинства антибиотиков пенициллиновой группы?
A) Гистамин
B) Аминобензол
C) Каприламин
D) 6-Аминопенициллановая кислота
D
9. Верно ли утверждение, что анилин обладает высокими антикоррозионными свойствами?
A) Да, верно
B) Нет, неверно
C) Анилин не влияет на коррозию
D) Анилин ускоряет коррозию
B
10. Где применяются амины в промышленности?
A) Только в парфюмерии
B) Только в лакокрасочной отрасли
C) В основном используются как пищевые добавки
D) Широко используются в производстве красок, резины, лекарственных препаратов
D
Заключение
Мы рассмотрели значимую группу азотсодержащих соединений — амины. Амины бывают трёх типов: первичные, вторичные и третичные, в зависимости от числа углеводородных радикалов, находящихся у атома азота. Изучили структуру аминов, определяющую их основные свойства и способность вступать в реакции с кислотами, образуя аммонийные соли. Определили основной механизм синтеза аминов посредством алкилирования аммиака или самих аминов галогеналканами. Помимо прочего, разобрали нюансы реакций нитрования и восстановления нитропроизводных, используемых для получения ароматических аминов.
Автор:
Щерба Тарас, методист «100балльного репетитора» по химии ЕГЭ