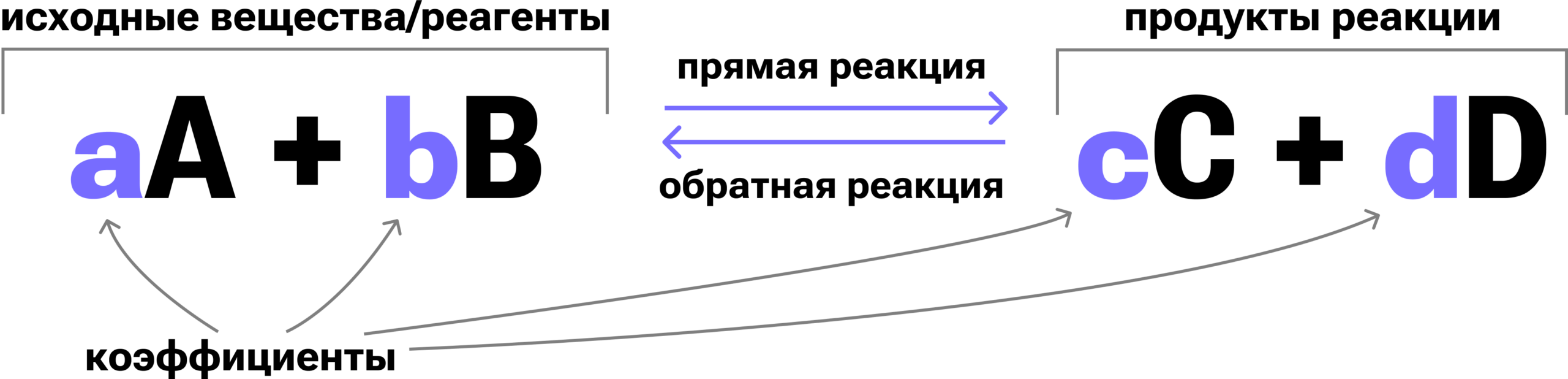
Введение
Значительное число химических реакций, встречающихся как в природных условиях, так и в промышленности, относятся к обратимым. Сущность этого явления заключается в сопряжённом протекании реакции образования продуктов и обратной реакции их распада до исходных веществ. Качественным и количественным описанием таких систем занимается раздел химической термодинамики, изучающий состояниехимического равновесия.
Особую практическую важность представляет не только само состояние равновесия, но и возможность управлять им. Это позволяет, к примеру, целенаправленно повышать выход целевого продукта в ключевых промышленных процессах.
В рамках статьи обратим внимание на:
- условия возникновения химического равновесия: какие реакции относятся к обратимым;
- методы управления равновесным состоянием химических систем через изменение внешних параметров;
- алгоритм и правила расчёта равновесных концентраций участников реакции.
Химическое равновесие
Понятие «химическое равновесие» относится к обратимым реакциям.
Обратимые реакции 一 химические реакции, которые протекают и в прямом, и в обратном направлениях (⇄).
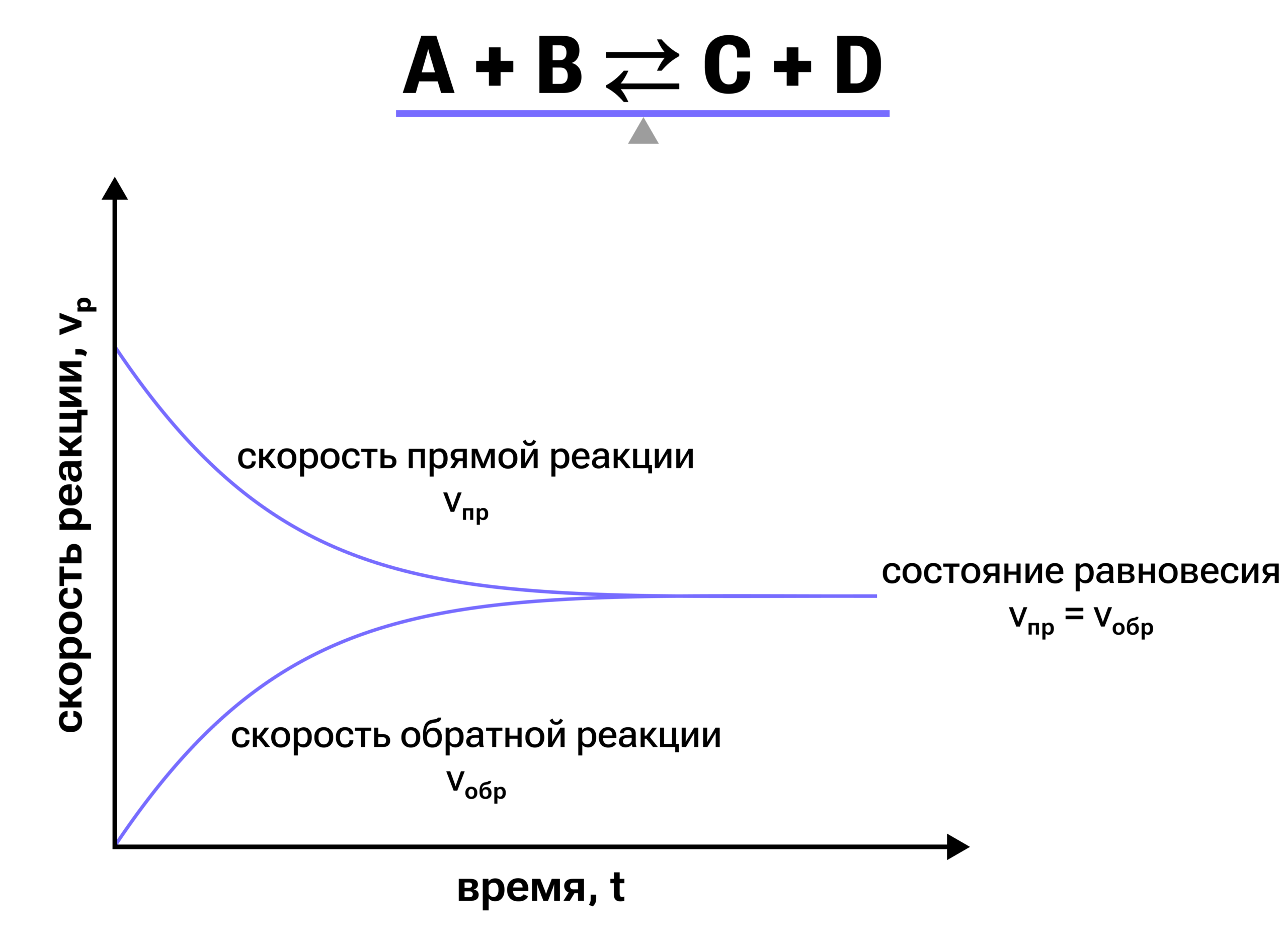
Химическое равновесие 一 состояние обратимой реакции, при котором скорость прямой реакции равна скорости обратной реакции, ввиду чего с течением времени количества веществ/концентрации участников реакции не изменяются.
Для обратимых химических реакций изначально высокая скорость превращения исходных веществ постепенно уменьшается из-за снижения концентрации реагентов. Одновременно с этим скорость обратной реакции, равная нулю в начале, увеличивается по мере накопления продуктов в системе. Равновесие достигается в тот момент, когда скорости этих разнонаправленных процессов совпадают. Концентрации компонентов системы при этом стабилизируются и сохраняют неизменные значения.
Под равновесными концентрациями понимают стабильные, не изменяющиеся во времени значения концентраций всех веществ в равновесной системе.
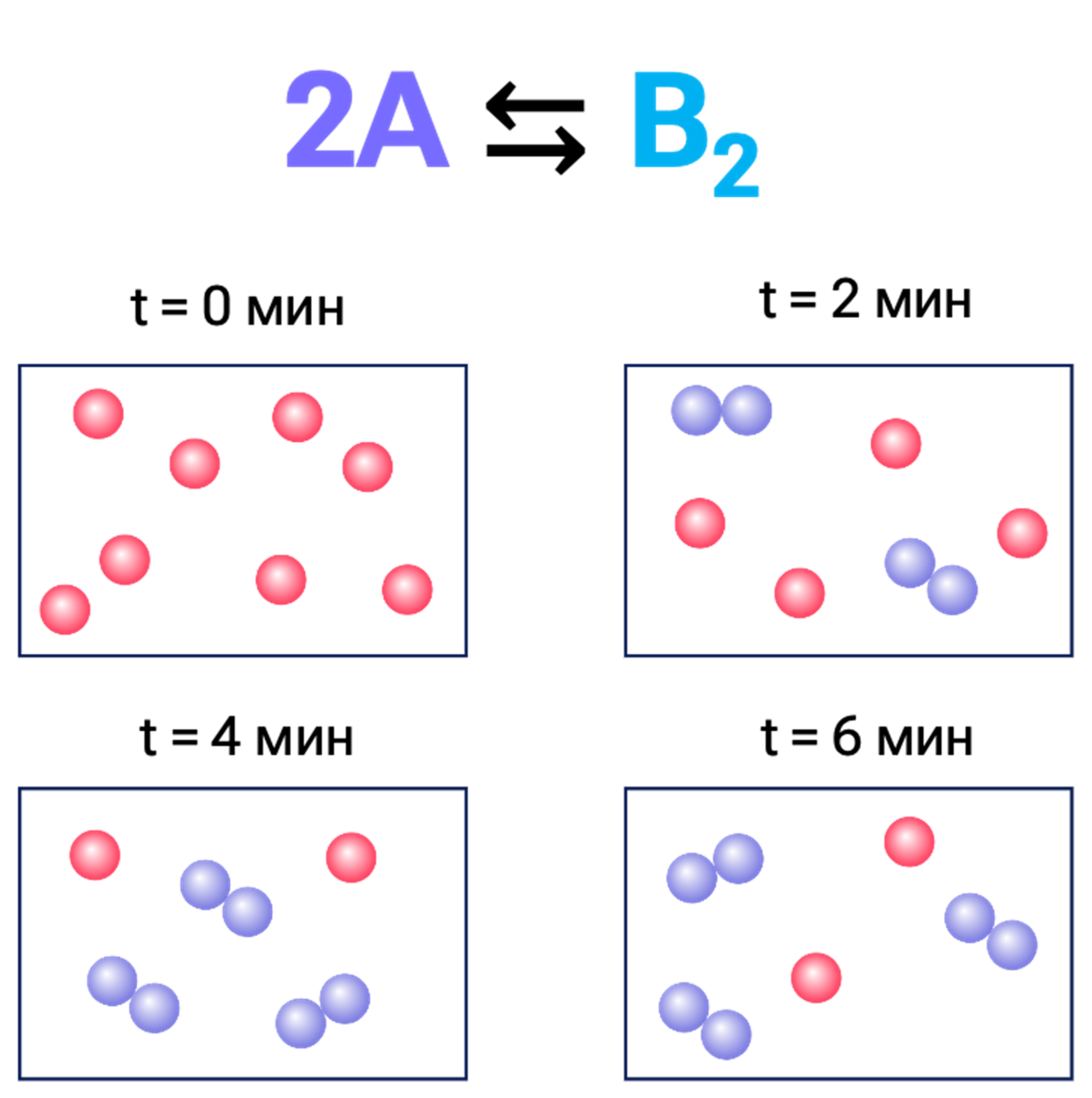
Обязательным этапом протекания любой обратимой реакции является достижение точки химического равновесия. В этом состоянии макроскопические изменения прекращаются: реагенты перестают расходоваться, а продукты — образовываться.
Нарушить установившееся равновесие можно, регулируя параметры системы: температурный режим процесса, давление в закрытой системе либо концентрации веществ, которые уаствуют в реакции.
Однозначное определение направления, в котором смещается химическое равновесие под действием внешних факторов, возможно благодаря использованию принципа Ле Шателье.
Принцип Ле Шателье: если на равновесную систему оказывать внешнее воздействие, то равновесие смещается в сторону той реакции (прямой или обратной), которая ослабляет это воздействие.
1. Изменение температуры
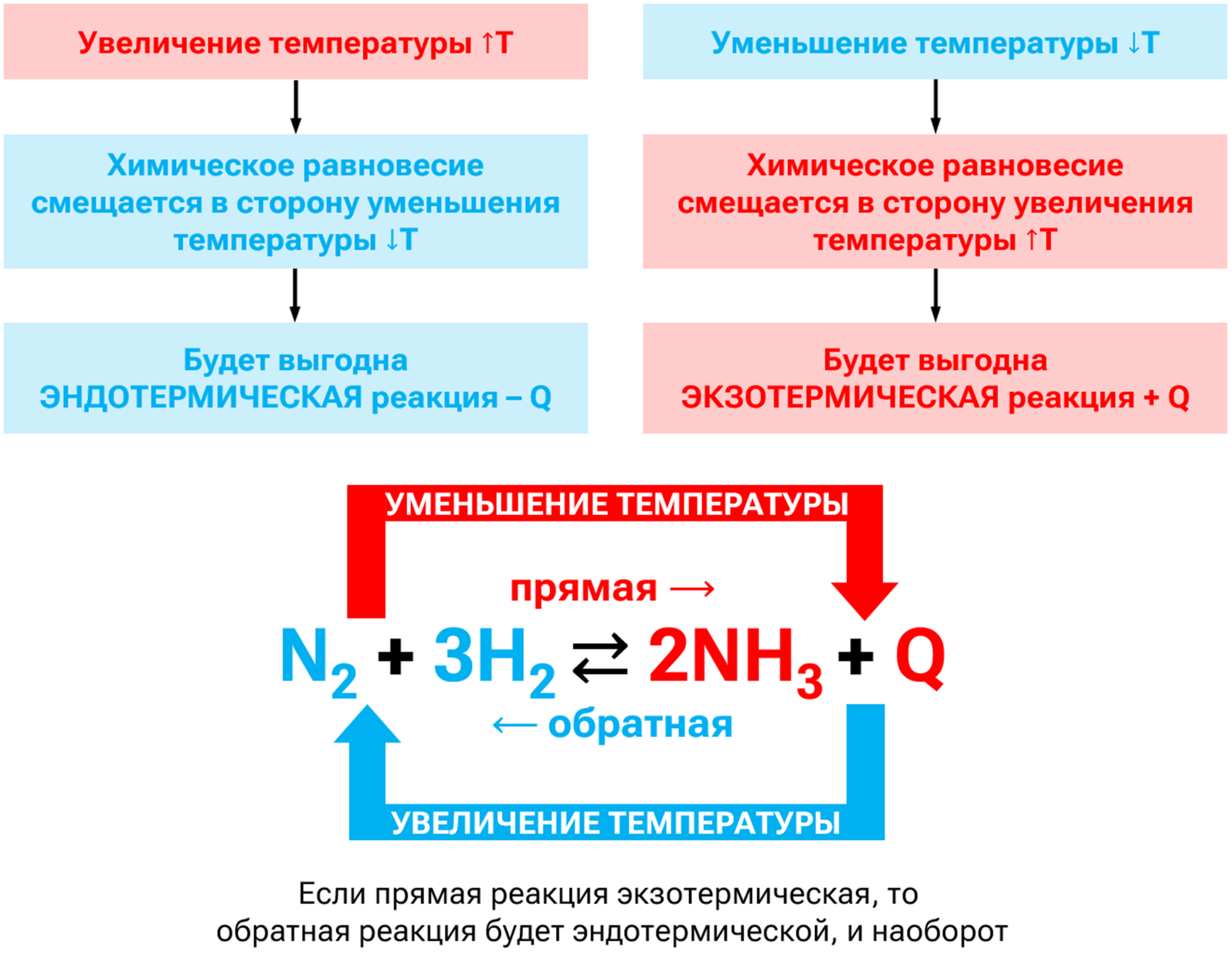
При увеличении температуры равновесие смещается в сторону эндотермического процесса, который сопровождается поглощением тепловой энергии. И наоборот, понижение температуры благоприятствует экзотермической реакции, при которой теплота выделяется.
Прямая и обратная реакции характеризуются равными по модулю, но противоположными по знаку тепловыми эффектами. В каком направлении смещается равновесие, зависит от знака теплового эффекта прямой реакции: для экзотермических процессов (Q > 0) нагревание смещает его в сторону реагентов, а для эндотермических (Q < 0) — в сторону продуктов.
2. Изменение давления (объёма)
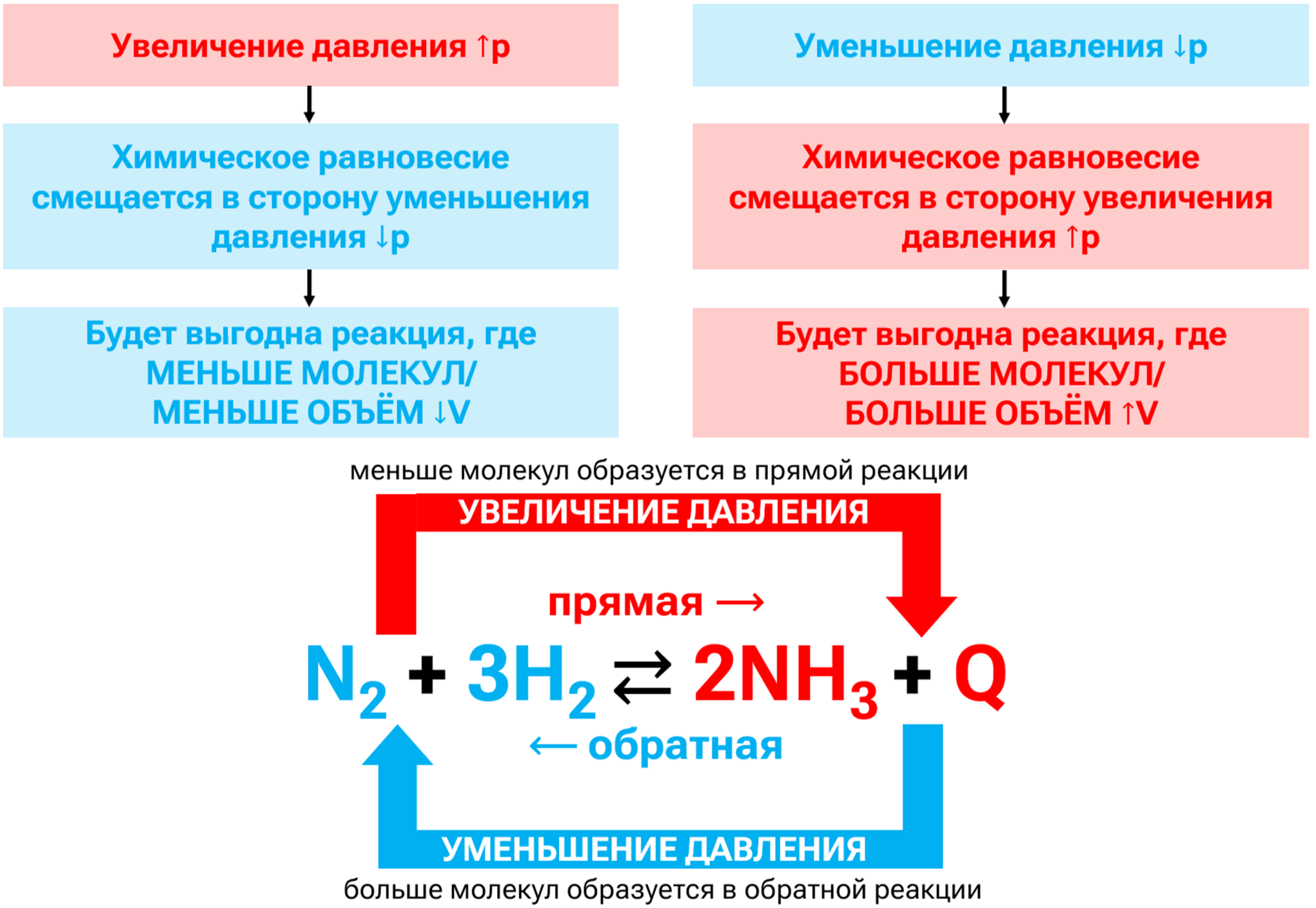
Давление оказывает влияние на положение химического равновесия исключительно в газофазных системах, и только если в системе при реакции происходит изменение общего числа молекул.
Рост давления способствует протеканию реакции с уменьшением общего числа молекул газа, что приводит к сокращению объёма системы. Уменьшение давления, напротив, смещает равновесие в сторону реакции с увеличением количества молекул газа и, следовательно, увеличением занимаемого этими молекулами объёма.
В системах, где все участники реакции находятся в конденсированном состоянии (твёрдом или жидком), варьирование давления практически не приводит к смещению равновесия вследствие пренебрежимо малой сжимаемости этих фаз.
Если в реакции количество молей газов с разных сторон от знака ⇄ одинаково, то оказывать влияние на положение равновесия давление не будет. Изменяя давление или объём реактора, можно добиться смещения равновесия исключительно в системах с участием реагентов и/или продуктов, находящихся в газовой фазе, и только при изменении общего числа молей газов в ходе реакции.
Важно для понимания: как следует из закона Бойля-Мариотта (известного вам из курса школьной физики), при постоянной температуре объём газа обратно пропорционален давлению. Поэтому варьирование объёма реакционной системы оказывает такое же влияние на положение равновесия, как и изменение давления, смещая его в сторону компенсирующего процесса.
3. Изменение количества вещества (концентрации)
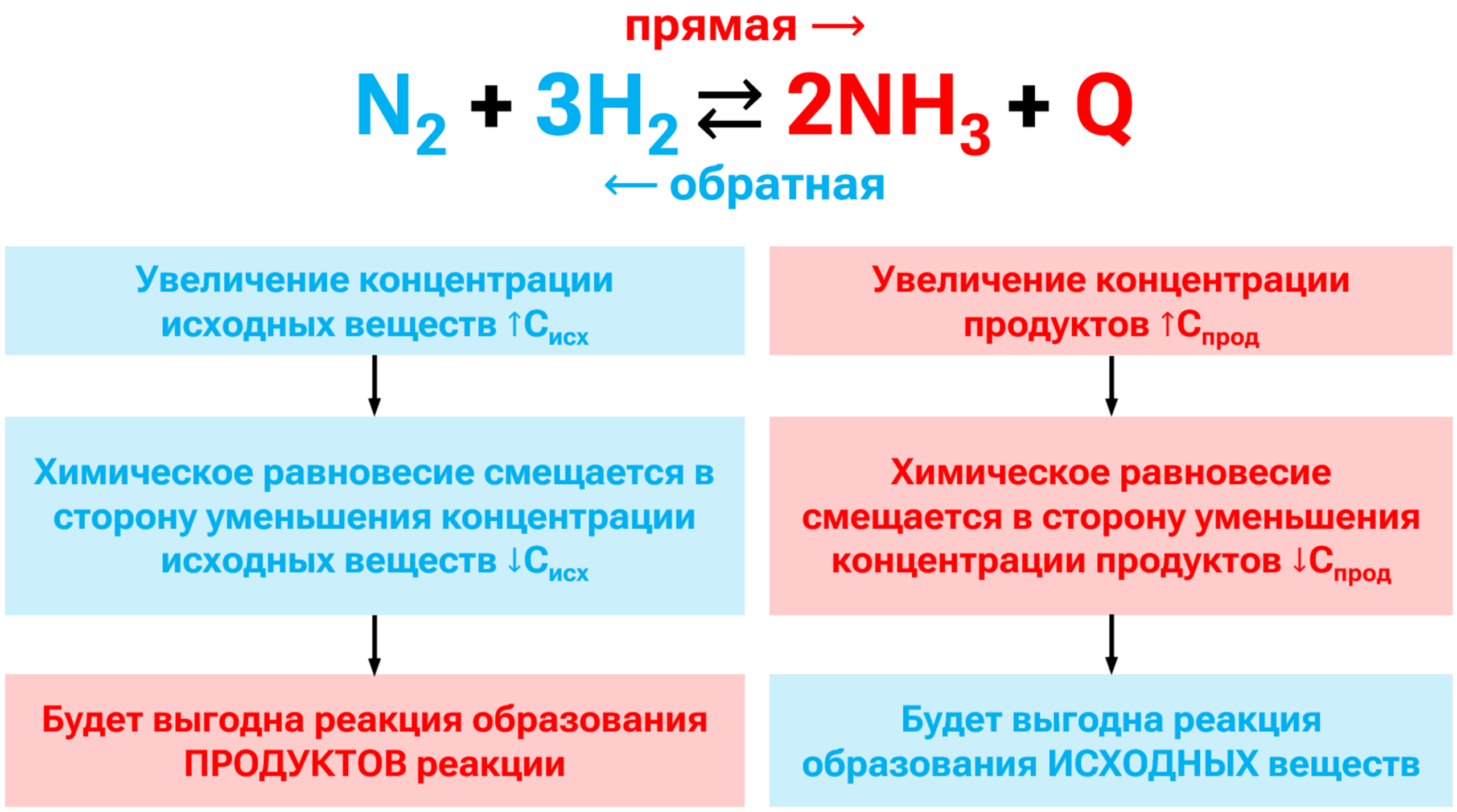
Увеличение концентрации реагентов или искусственное снижение концентрации продуктов (например, их удаление из реактора) инициирует смещение равновесия в сторону прямой реакции. Это объясняется тем же принципом компенсации внешних воздействий: прямая реакция приводит к расходованию реагентов и преобразованию их в продукты.
Аналогично, создание избытка продуктов или дефицита реагентов направляет процесс в сторону обратной реакции, активирующей расходование продуктов и восполнение реагентов.

Смещение химического равновесия при добавлении дополнительного вещества
Рассмотрим реакцию этерификации:
HCOOH + CH₃OH ⇄ HCOOCH₃ + H₂O.
В какую сторону можно ожидать смещения равновесия при добавлении KOH?
KOH не является прямым участником реакции этерификации, но вступает во взаимодействие с муравьиной кислотой, уменьшая её концентрацию в системе. Такое косвенное участие добавленного в систему вещества приведёт к смещению химического равновесия согласно принципу Ле Шателье:
HCOOH + KOH = HCOOK + H₂O
Уменьшение концентрации HCOOH вследствие реакции с KOH приводит к смещению равновесия в сторону обратной реакции. Таким образом, система стремится компенсировать потерю кислоты, увеличивая скорость процесса её образования.
Важно отметить, что катализатор, при его внесении в систему, не оказывает влияния на положение химического равновесия, а только ускоряет его установление благодаря синхронному повышению скоростей прямой и обратной реакций.

Примеры:

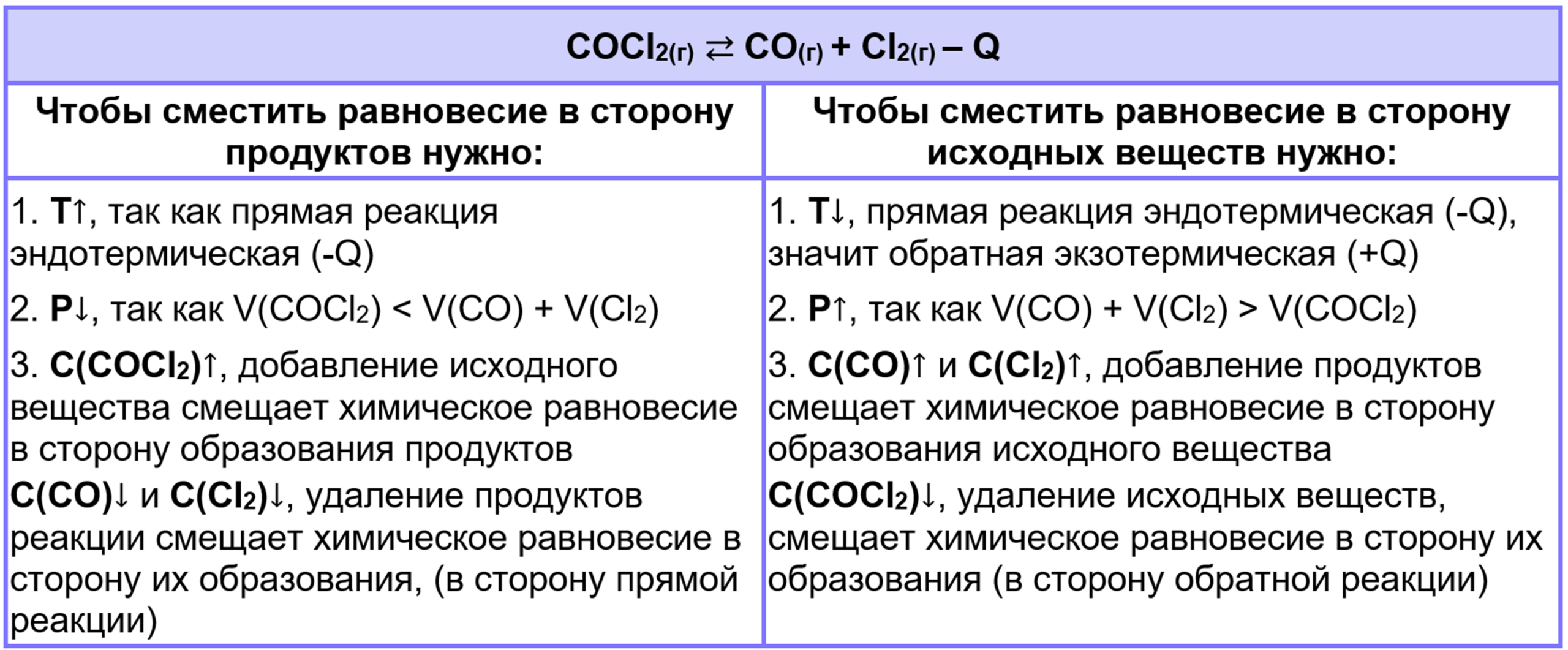
Расчёт равновесных концентраций
Любая химическая реакция подчиняется закону сохранения массы, поэтому расчёт количества вещества участников реакции в состоянии равновесия мало чем отличается от аналогичных расчётов для необратимых реакций.
Рассмотрим в качестве примера типичную реакцию, встречающуюся в задании №23 ЕГЭ по химии:
2NO(г) + O₂(г) ⇄ 2NO₂(г)
В условии говорится, что в реактор постоянного объёма внесли смесь NO и O₂. Начальная концентрация кислорода составляла, например, 0,5 моль/л. После установления равновесия в системе оказалось, что концентрации NO и O₂ равны 0,4 моль/л и 0,1 моль/л соответственно. Необходимо вычислить равновесную концентрацию NO₂ и определить, какой была исходная концентрация NO.
Для количественного описания равновесия применяются: начальная (исходная) концентрация участников реакции, их конечная равновесная концентрация и разность этих значений 一 то количество данного вещества, которое прореагировало/образовалось в системе. Построим для удобства таблицу, в ячейки которой будем вносить известные нам значения:

Можем сразу внести исходную концентрацию NO₂. В данном случае, исходная концентрация продукта реакции равна 0 моль/л, поскольку его не поместили в реактор. Если же продукты равновесной реакции были в реакционном сосуде изначально, их концентрации не равны 0 моль/л.
Кроме того, нам известны исходная концентрация O₂ и равновесные концентрации NO и O₂.
После внесения всех известных нам значений в таблицу стало видно, что в ходе установления химического равновесия в системе закономерно уменьшилась концентрация исходного вещества 一 O₂. Это значит, что определённое количество кислорода при этом прореагировало, и мы можем найти это значение как разность исходной и равновесной концентраций:
C(прор. O₂) = C(исх. O₂) – C(равн. O₂) = 0,5 – 0,1 = 0,4 моль/л
n(прор. O₂) = 0,4 моль
Именно столько кислорода и вступило в реакцию к моменту установления химического равновесия. Вещества, как мы помним, вступают в химические реакции в соотношениях, определяемых коэффициентами в химическом уравнении реакции. Пользуясь этим правилом, можем рассчитать количества вещества NO и NO₂ по уравнению реакции:
n(прор. NO) = 2n(прор. O₂) = 2 · 0,4 = 0,8 моль
n(обр. NO₂) = 2n(прор. O₂) = 2 · 0,4 = 0,8 моль
После расчётов по уравнению реакции, мы заполнили практически все ячейки таблицы, осталось найти лишь искомые концентрации.
Равновесная концентрация NO₂ 一 это концентрация образовавшегося продукта, отсутствовавшего в системе до начала реакции. Поскольку реактор имеет постоянный объём, концентрации веществ в нём численно равны количествам вещества:
C(обр. NO₂) = 0,8 моль/л
Чтобы найти исходную концентрацию NO, суммируем его равновесное количество (равное концентрации в состоянии равновесия) и количество прореагировавшего вещества:
n(исх. NO) = n(равн. NO) + n(прор. NO) = 0,4 + 0,8 = 1,2 моль
C(исх. NO) = 1,2 моль/л

Вот и всё, оставшиеся значения внесены в таблицу и задача решена.
Мы можем наблюдать смещение химического равновесия и в повседневной жизни. Когда открывается бутылка газировки, часть растворённого CO₂ быстро выходит из раствора. Это связано с тем, что равновесие в следующей реакции смещено:
H₂O(ж) + CO₂(г) ⇄ H2CO₂(ж).
Продукт реакции — крайне неустойчивая угольная кислота, которая способна разлагаться на образующие её вещества 一 углекислый газ и воду. При уменьшении давления газа над жидкостью система реагирует, уменьшая концентрацию растворённого CO₂ 一 угольная кислота начинает бурно разлагаться. Закрытая бутылка поддерживает равновесие, пока давление не меняется.
Заключение
Таким образом, практическая важность изучения явления химического равновесия заключается в возможности управлять положением равновесия путём, направленно изменяя внешние условия 一 концентрацию реагентов, температуру или давление. Принцип Ле Шателье служит надёжным теоретическим основанием для предсказания направленности смещения равновесия и оптимизации технологических процессов с целью максимизации выхода целевых продуктов. Современные компьютерные методы расчёта позволяют с высокой точностью прогнозировать состав системы в состоянии равновесия, что имеет фундаментальное значение для химической термодинамики, кинетики и промышленного катализа.
Знания о химическом равновесии и обратимых реакциях важны для понимания химии. Именно поэтому в первой части КИМ ЕГЭ по химии есть два задания, посвящённые этой теме 一 №22 и №23. После прочтения данной статьи вы узнали всё, что нужно знать о химическом равновесии для экзамена.
Автор:
Щерба Тарас, методист «100балльного репетитора» по химии ЕГЭ