Введение
В этой статье рассмотрим ковалентную химическую связь, её виды и механизмы образования, а также степень окисления и валентность элементов. Тема тесно связана со строением атома и электронной конфигурацией, поэтому важно понимать не только правила, но и их логику.
По шагам разберём:
- как образуется ковалентная связь,
- чем отличается полярная от неполярной,
- как работает донорно-акцепторный механизм,
- как считать степени окисления и определять валентность.
В конце посмотрим, как эти знания применяются в заданиях экзамена.
Где эта тема встречается в экзаменационных заданиях
Знание химических связей и характеристик атомов напрямую проверяется в двух заданиях единого государственного экзамена:
- Задание 3 проверяет умение работать со степенями окисления: определять их значения, устанавливать максимальные и минимальные, а также находить разницу между ними. В заданиях могут предлагаться формулировки, где нужно сопоставить элементы по одинаковым степеням окисления в составе ионов или по совпадающей разности между крайними значениями.
- Задание 4 связано с анализом строения веществ. Здесь требуется определить типы химической связи в предложенных веществах, например выявить наличие ковалентной неполярной связи или найти соединения, в которых одновременно присутствуют ионные и ковалентные связи.
Без понимания теории эти задания решаются плохо, поэтому дальше разберём всё по порядку.

Ковалентная связь и её разновидности
Ковалентная связь — это химическая связь, которая образуется за счёт перекрывания (или обобществления) пары валентных электронных облаков взаимодействующих атомов, таким образом происходит формирование общей электронной пары. Она удерживает вместе атомы в молекулах простых веществ, сложных веществ и в узлах атомных кристаллических решёток.
Полярная и неполярная ковалентная связь
Различают два основных вида такого взаимодействия:
Ковалентная неполярная связь возникает между атомами одного и того же химического элемента-неметалла. Поскольку атомы абсолютно одинаковы, их разность электроотрицательностей равна нулю. Общая электронная плотность распределяется между ними строго равномерно, не сдвигаясь ни в одну из сторон.
Примеры простых веществ: водород ($H_2$), азот ($N_2$), кислород ($O_2$), фтор ($F_2$), хлор ($Cl_2$), бром ($Br_2$), иод ($I_2$), белый фосфор ($P_4$), сера ($S_8$), а также углерод в виде алмаза или графита.
Важно: неполярная связь может быть не только в простых веществах, но и внутри сложных молекул, если связаны одинаковые атомы. Примеры веществ с такими «внутренними» неполярными связями:
- Пероксиды: пероксид водорода ($H_2O_2$) имеет структуру $H−O−O−H$. Связь между двумя атомами кислорода является неполярной.
- Карбиды и ацетилениды: карбид кальция ($CaC_2$).
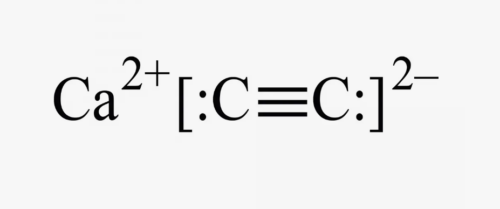
- Сульфиды со структурой дисульфида: пирит ($FeS_2$).
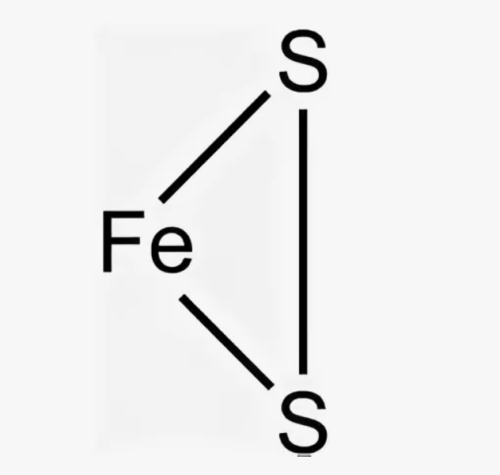
- Органические соединения: связь $C−C$ в этане ($CH_3−CH_3$), этилене или ацетилене ($CH \equiv CH$).
Ковалентная полярная связь возникает между атомами разных неметаллов. Из-за различий в электроотрицательности электронная плотность смещается к атому, который сильнее притягивает электроны.
Примеры молекул: хлороводород ($HCl$), вода ($H_2O$), аммиак ($NH_3$), метан ($CH_4$), углекислый газ ($CO_2$), серный ангидрид ($SO_3$).
Механизмы образования ковалентной связи
В зависимости от того, как атомы предоставляют электроны для формирования общей пары, различают обменный и донорно-акцепторный механизмы.
Обменный механизм предполагает равное участие атомов: каждый из них вносит по одному неспаренному электрону. При их объединении образуется общая электронная пара, которая и обеспечивает связь между атомами.
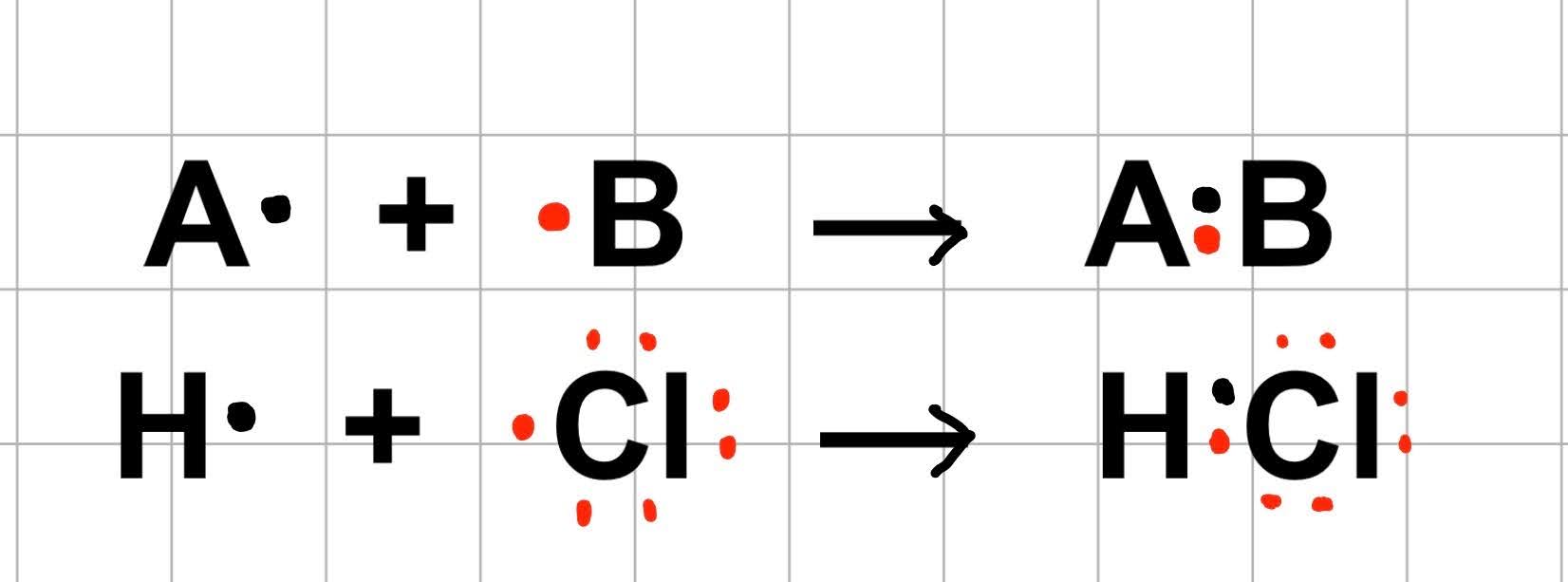
Донорно-акцепторный механизм работает иначе. В нём один атом (донор) предоставляет уже готовую, неподелённую пару электронов. Второй атом (акцептор) предоставляет только пустую орбиталь, на которую эта пара размещается.
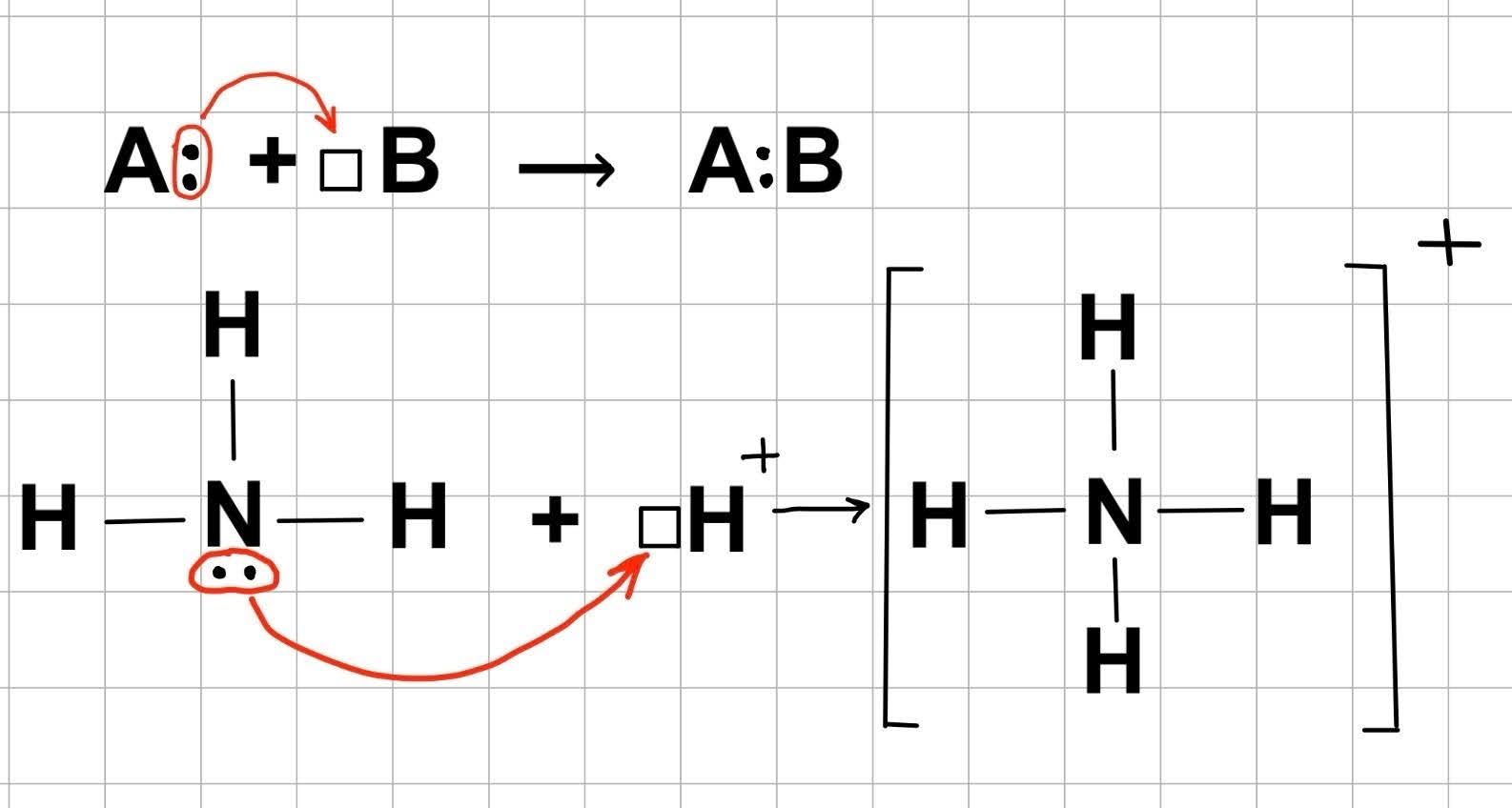
Запомни основные классы и частицы, внутри которых присутствует донорно-акцепторная связь:
- Катион аммония $NH_4^+$ и абсолютно все его соли (хлорид аммония $NH_4Cl$, сульфат аммония $(NH_4)_2SO_4$).
- Катион фосфония $PH_4^+$ и соли фосфония.
- Угарный газ (оксид углерода(II)) $CO$. В молекуле тройная связь, из которой две связи образованы по обменному механизму, а третья по донорно-акцепторному.
- Озон $O_3$.
- Азотная кислота $HNO_3$ и все нитраты (например, $NaNO_3$).
- Комплексные соединения — связь между центральным атомом металла и лигандами (тетрагидроксоалюминат натрия $Na[Al(OH)_4]$, тетрагидроксоцинкат калия $K_2[Zn(OH)_4]$).
Характеристики ковалентной связи: полярность и энергия
Ковалентная связь характеризуется такими параметрами, как полярность, энергия, кратность и длина.
Полярность связи определяется разностью электроотрицательностей связываемых атомов. Чем дальше элементы стоят друг от друга в таблице Менделеева по значению электроотрицательности, тем выше полярность связи. Обрати внимание, что полярность связи и полярность всей молекулы могут не совпадать. Например, в молекуле углекислого газа $CO_2$ связи $C=O$ сильно полярны, но сама молекула имеет линейное строение, векторы компенсируют друг друга, поэтому молекула в целом неполярна. Вода $H_2O$ имеет угловое строение, и векторы не компенсируются, поэтому молекула воды является полярной.
Энергия связи показывает прочность молекулы. Это количество энергии, которое нужно затратить на разрыв химической связи. Кратные связи (двойные и тройные) имеют намного большую энергию и меньшую длину, чем одинарные. Сравни молекулу азота $N \equiv N$ с тройной связью (энергия 946 кДж/моль, длина 0,110 нм) и молекулу фтора $F−F$ с одинарной связью (энергия 159 кДж/моль, длина 0,142 нм). Именно высокая энергия тройной связи делает газообразный азот химически инертным при обычных условиях.
Кратность связи показывает, сколько общих электронных пар соединяет два атома. Чем больше таких пар, тем прочнее связь и тем меньше её длина.
Длина связи показывает, как далеко находятся друг от друга ядра связанных атомов. Чем больше радиусы атомов — тем длиннее связь, а чем выше кратность — тем она короче.
Степень окисления атомов
Степень окисления показывает условный заряд атома в веществе. Его рассчитывают, предполагая, что все связи полностью ионные. Значение всегда указывается со знаком «плюс» или «минус», а в простых веществах оно равно нулю.
Высшая и низшая степени окисления
Высшая (максимально положительная) степень окисления обычно совпадает с номером группы короткого варианта периодической таблицы.
Исключения: фтор (у него вообще нет положительных степеней окисления, только 0 и −1), кислород (максимум +2 во фториде кислорода $OF_2$), медь (элемент I группы, но проявляет +2), золото (элемент I группы, но проявляет +3).
Низшая (минимально отрицательная) степень окисления для неметаллов рассчитывается по формуле «номер группы минус 8». Например, для хлора (VII группа) расчёт выглядит так: 7 − 8 = −1. Для всех металлов низшая степень окисления всегда равна нулю, так как металлы не способны принимать электроны и приобретать отрицательный заряд.
Правила расчёта степени окисления
Чтобы уверенно решать задания, используй чёткий алгоритм:
- В нейтральной молекуле сумма степеней окисления всех атомов всегда равна нулю.
- В сложном ионе сумма степеней окисления всех атомов равна заряду самого иона.
- Водород в соединениях с неметаллами имеет заряд +1. Исключение составляют гидриды активных металлов ($NaH$, $CaH_2$), где водород проявляет степень окисления −1.
- Кислород почти всегда проявляет степень окисления −2. Исключения включают пероксиды ($H_2O_2$, где кислород −1) и фторид кислорода ($OF_2$, где кислород +2).
- Щелочные металлы всегда отдают один электрон (заряд +1), металлы второй группы главной подгруппы и цинк отдают два электрона (заряд +2), алюминий всегда имеет степень окисления +3. Фтор всегда электроотрицателен, его заряд строго −1.
Сводная таблица типичных степеней окисления неметаллов
| Элементы (группа) | Низшая степень | Характерные промежуточные | Высшая степень |
|---|---|---|---|
| Галогены (Cl, Br, I, VII группа) | −1 | +1, +3, +5 | +7 |
| Халькогены (S, Se, VI группа) | −2 | +4 | +6 |
| Пниктогены (N, P, V группа) | −3 | +1, +2, +3, +4 | +5 |
| Углерод и кремний (C, Si, IV группа) | −4 | +2 | +4 |
Пример с решением: расчёт степени окисления пошагово
Посмотрим алгоритм на примере трёх различных веществ.
Пример 1
Найдём степень окисления хрома в дихромате калия ($K_2Cr_2O_7$).
- Выставляем постоянные заряды. Калий относится к щелочным металлам, его заряд +1. Кислород имеет заряд −2.
- Обозначаем неизвестный заряд хрома за $x$.
- Составляем уравнение так, чтобы сумма была равна нулю: $2 \cdot (+1) + 2 \cdot x + 7 \cdot (−2) = 0$.
- Решаем уравнение. Раскрываем скобки: 2 + 2x − 14 = 0. Получаем 2x = 12. Значит, x = +6.
Ответ: степень окисления хрома равна +6.
Пример 2
Найдём степень окисления серы в серной кислоте ($H_2SO_4$).
- Водород с неметаллами имеет заряд +1, кислород −2.
- Заряд серы примем за $x$.
- Уравнение суммарного заряда: $2 \cdot (+1) + x + 4 \cdot (−2) = 0$.
- Рассчитываем значение: 2 + x — 8 = 0, откуда x = +6.
Ответ: степень окисления серы равна +6.
Пример 3
Найдём степень окисления азота в катионе аммония ($NH_4^+$).
- Перед нами ион с зарядом +1. Следовательно, сумма зарядов атомов будет равна не нулю, а +1.
- Водород положительный (+1). Азот обозначаем за $x$.
- Составляем уравнение: $x + 4 \cdot (+1) = +1$.
- Находим корень: x + 4 = 1, значит x = −3.
Степень окисления азота в этом катионе −3. Проверка: подставим значение обратно. −3 + 4 = +1. Совпадает с зарядом иона.
Валентность химических элементов
Валентность показывает, сколько химических связей атом данного элемента может образовать с другими атомами.
В отличие от степени окисления, валентность указывает на реальное количество общих электронных пар. У валентности нет знака («плюс» или «минус»). Кроме того, валентность элементов в соединениях никогда не может быть равной нулю. Численные показатели валентности и заряда часто совпадают, но существуют важные исключения. Яркий пример — молекула азота $N_2$. В ней атомы азота связаны тройной связью, поэтому валентность каждого атома равна III. При этом степень окисления в простом веществе равна 0.
Высшая и низшая валентность неметаллов
Высшая валентность элемента обычно численно равна номеру группы в периодической системе. Но есть важные исключения, у которых высшая валентность не равна номеру группы:
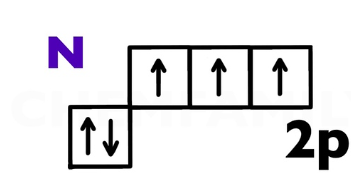
- Азот (N). Находится в V группе. Его высшая степень окисления равна +5, но его высшая валентность равна только IV. Азот физически не может образовать пять связей, так как у него отсутствует вакантный d-подуровень для распаривания электронов.
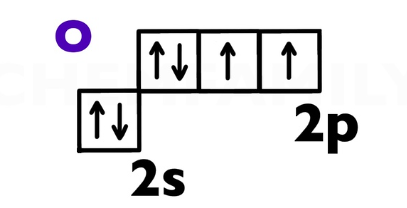
- Кислород (O). Расположен в VI группе. Максимальная возможная валентность кислорода равна II, и только в редких случаях (в ионе гидроксония $H_3O^+$ или в молекуле угарного газа $CO$) она дорастает до III.
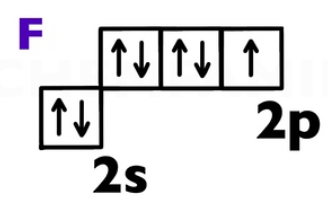
- Фтор (F). Расположен в VII группе, но может образовать лишь одну связь. Его валентность строго равна I.
Пример с решением: алгоритм расчёта валентности
Чтобы вычислить валентность в бинарном соединении, помни простое правило: валентность атома × число его атомов = валентность другого атома × число его атомов.
Пример 1
Определим валентность углерода в оксиде углерода(IV) ($CO_2$).
- Кислород в оксидах всегда двухвалентен (II).
- Найдём сумму единиц валентности для кислорода: $2 \text{ атома} \cdot \text{II} = 4$.
- Следовательно, на один атом углерода приходится 4 единицы. Разделим 4 на количество атомов углерода (1 атом): $4 / 1 = 4$.
Ответ: валентность углерода равна IV.
Пример 2
Определим валентность углерода в метане ($CH_4$).
- Водород обладает единственным неспаренным электроном, он одновалентен (I).
- Сумма для водорода: $4 \text{ атома} \cdot \text{I} = 4$.
- Углерод в молекуле один. Разделим 4 на 1.
Ответ: валентность углерода равна IV.
Пример 3
Определим валентность азота в аммиаке ($NH_3$).
- Водород одновалентен (I).
- Общая сумма единиц: $3 \text{ атома} \cdot \text{I} = 3$.
- На один атом азота приходится 3 единицы.
Ответ: валентность азота равна III.
Понятия «высший оксид» и «высший гидроксид»
Высший оксид элемента содержит этот элемент в максимальной положительной степени окисления (которая, как правило, равна номеру группы). Например, для серы (VI группа) это будет оксид, в котором сера проявляет +6. Формула высшего оксида серы имеет вид $SO_3$. Для хлора (VII группа) высший оксид содержит хлор в степени окисления +7, его формула $Cl_2O_7$.
Высший гидроксид напрямую генетически соответствует высшему оксиду. В нём центральный атом сохраняет ту же самую высшую степень окисления. Если речь идёт о металлах первой или второй групп, то гидроксид представляет собой основание (например, натрию с зарядом +1 соответствует $NaOH$, а барию с зарядом +2 соответствует $Ba(OH)_2$). Если мы говорим о неметаллах, то их высшими гидроксидами являются кислородсодержащие кислоты.
Примеры соответствий:
- Углерод: высший оксид $CO_2$ (+4) $\rightarrow$ высший гидроксид $H_2CO_3$ (+4).
- Сера: высший оксид $SO_3$ (+6) $\rightarrow$ высший гидроксид $H_2SO_4$ (+6).
- Хлор: высший оксид $Cl_2O_7$ (+7) $\rightarrow$ высший гидроксид $HClO_4$ (+7).
Практика: решение заданий ЕГЭ с объяснением
Рассмотрим, как применять полученные знания в условиях реального тестирования.
Задание 3. Поиск анионов с одинаковой степенью окисления
Условие
Предложен ряд химических элементов: 1) N, 2) S, 3) Mo, 4) Zn, 5) C. Из числа указанных в ряду элементов выберите два элемента, которые в составе образованных ими анионов с общей формулой $ЭO_x^{2−}$ могут иметь одинаковую степень окисления.
- Обращаем внимание на формулу аниона из условия: $ЭO_x^{2−}$. Это означает, что заряд самого иона равен 2−. Нам нужно составить самые известные кислотные остатки для элементов из списка.
- Анализируем каждый элемент.
- Азот образует нитрат-ион $NO_3^−$ и нитрит-ион $NO_2^−$. У них заряд 1−. Формату не соответствуют.
- Сера образует сульфат-ион $SO_4^{2−}$ (соответствует формату). Рассчитаем заряд серы в нём: $x + 4 \cdot (−2) = −2$, откуда $x − 8 = −2$, следовательно $x = +6$.
- Молибден находится в VI побочной группе (аналог хрома) и образует молибдаты. Анион $MoO_4^{2−}$. Степень окисления молибдена: $x + 4 \cdot (−2) = −2$, получается $x = +6$.
- Цинк даёт цинкаты, например, анион $ZnO_2^{2−}$. Его степень окисления всегда +2 (расчёт: $x + 2 \cdot (−2) = −2 \rightarrow x − 4 = −2 \rightarrow x = +2$).
- Углерод формирует карбонат-ион $CO_3^{2−}$. Степень окисления C: $x + 3 \cdot (−2) = −2 \rightarrow x − 6 = −2 \rightarrow x = +4$.
- Сопоставляем результаты. Анионы с зарядом 2− дают сера, молибден, цинк и углерод, однако только сера (2) и молибден (3) в этих ионах имеют одинаковую степень окисления, которая равна +6.
Ответ: 23.
Задание 3. Разность степеней окисления
Условие
Предложен ряд элементов: 1) Se, 2) F, 3) Al, 4) Ca, 5) N. Определите, какие из указанных элементов имеют одинаковую разность между значениями их высшей и низшей степеней окисления. Запишите номера двух выбранных элементов.
- Для каждого элемента необходимо выписать высшую и низшую степени окисления, используя правила.
- Проводим расчёт.
- Селен (VI группа). Высшая: +6. Низшая для неметалла (6 — 8): −2. Разность составит: $6 − (−2) = 8$.
- Фтор (VII группа, исключение). Высшая равна 0. Низшая: −1. Разность: $0 − (−1) = 1$.
- Алюминий (III группа). Высшая: +3. Низшая: 0. Разность: $3 − 0 = 3$.
- Кальций (II группа, металл). Высшая: +2. Низшая для металла: 0. Разность: $2 − 0 = 2$.
- Азот (V группа). Высшая: +5. Низшая (5 — 8): −3. Разность: $5 − (−3) = 8$.
- Одинаковую разность, равную 8, имеют селен (1) и азот (5).
Ответ: 15.
Задание 4. Полярность и неполярность ковалентной связи в веществах
Условие
Из предложенного перечня выберите два вещества, в которых присутствует ковалентная неполярная химическая связь: 1) алмаз, 2) ацетилен, 3) вода, 4) метан, 5) соль NaCl.
- Вспоминаем правило: ковалентная неполярная связь образуется между одинаковыми неметаллами. Она бывает как в простых веществах, так и внутри некоторых сложных молекул.
- Проверяем каждое вещество.
- Алмаз (состоит из атомов углерода C). Это простое вещество. Связи между атомами C-C абсолютно одинаковы, связь ковалентная неполярная. Подходит.
- Ацетилен (формула $C_2H_2$ или $HC \equiv CH$). Это сложное вещество, но между двумя атомами углерода существует тройная связь углерод-углерод. Атомы одинаковые, поэтому данная связь ковалентная неполярная. Подходит.
- Вода ($H_2O$). Состоит из атомов кислорода и водорода. Разные неметаллы формируют ковалентную полярную связь. Не подходит.
- Метан ($CH_4$). Углерод соединён с атомами водорода. Неметаллы разные, связь полярная. Не подходит.
- Фосфор белый ($P_4$). Простое вещество фосфор, атомы одинаковые. Связь ковалентная неполярная. Подходит.
- Соль $NaCl$ — ионная связь, не ковалентная. Не подходит.
- Под наши условия подходят варианты 1 и 2.
Ответ: 12.
Заключение
Ковалентная связь, степень окисления и валентность — это база, на которой держится большая часть школьной химии. Если здесь есть пробелы, дальше становится значительно сложнее.
В этой теме важно не просто запомнить правила, а понять логику:
- как распределяются электроны,
- почему возникает та или иная связь,
- откуда берутся степени окисления и валентности.
Тогда даже незнакомые задания решаются спокойно — через анализ, а не угадывание.
При подготовке к экзамену обращай внимание на типовые ситуации: определение типа связи, расчёт степеней окисления и сравнение элементов. Если ты уверенно разбираешься в этих вопросах, задания по теме перестают быть сложными.