Введение
Сера и её соединения занимают важное место в неорганической химии и регулярно встречаются в заданиях ЕГЭ. Чтобы уверенно справляться с ними, важно понимать химические свойства серы, её возможные степени окисления и особенности поведения в разных условиях.
Изучение этой темы позволяет разобраться в механизмах окислительно-восстановительных реакций, реакций нейтрализации и ионного обмена. Соединения серы образуют широкий круг веществ — от простого вещества до оксидов, кислот и солей, — и их свойства во многом определяются степенью окисления серы. Например, оксиды SO₂ и SO₃ проявляют разное химическое поведение в водных растворах именно из-за различия в степени окисления.
Кроме того, задания ЕГЭ часто проверяют способность определять типы связей в соединениях серы, разбираться в структуре молекул и решать качественные и количественные задачи.
Всё это напрямую связано с пониманием электронного строения атомов серы и закономерностей формирования связей в серосодержащих соединениях.
Помимо теории, экзамен требует умения применять знания на практике. Практические задания включают вычисление массовой доли вещества, молярной массы, объёмов газов и концентраций растворов, содержащих серу и её соединения. Систематическое закрепление материала позволит уверенно справляться с такими задачами.
Халькогены
Халькогены — элементы главной подгруппы VI группы периодической системы элементов Д. И. Менделеева. К ним относятся кислород (O), сера (S), селен (Se), теллур (Te) и полоний (Po).
Название образовано от греческих слов χαλκός («медь») и γενής («рождающий»), поскольку многие металлы образуют соединения именно с этими элементами, особенно часто встречается сульфидная форма минералов.
Химическая активность халькогенов
| Электронная конфигурация внешнего энергетического уровня | ns2np4 |
|---|---|
| Основные степени окисления кислорода | -2, -1, 0, +1, +2, т. е. высшая валентность и степень окисления не равны номеру группы |
| Основные степени окисления серы, селена и теллура | -2, 0, +4, +6 |
| Химическая активность | Кислород является сильным окислителем, сера — окислитель средней силы |
| Физические свойства | При н. у. кислород O2 — газ без цвета и запаха, сера — жёлтое твёрдое вещество, селен и теллур — тёмно-серое и светло-серое твёрдые вещества соответственно |
Физические свойства халькогенов


Сера
Степени окисления серы
| С. о. серы | -2 | -1 | 0 | +4 | +6 |
|---|---|---|---|---|---|
| Пример соединения | Сероводород и его соли | Дисульфиды | Простое вещество | Оксид серы(IV), сернистая кислота и её соли | Оксид серы(VI), серная кислота и её соли, фторид серы(VI) |
| Формула соединения | H2S, Na2S, FeS, NaHS | FeS2 | S или S8 | SO2, H2SO3, Na2SO3, NaHSO3 | SO3, H2SO4, Na2SO4, NaHSO4, SF6 |
Аллотропные модификации серы
Сера способна существовать в нескольких формах — аллотропных модификациях.
Аллотропия означает присутствие двух или более форм одного и того же химического элемента, отличающихся структурой или молекулярным составом.
При стандартных условиях наиболее стабильна ромбическая форма серы — твёрдый жёлтый кристаллический порошок. При повышении температуры появляется моноклинная разновидность серы, структура которой также состоит из молекул S8. Если быстро охладить жидкую серу, возникает третья модификация — пластическая сера, имеющая тёмно-коричневый оттенок. Несмотря на многообразие форм, самой устойчивой остаётся именно ромбическая сера, к которой постепенно переходят остальные модификации при комнатной температуре.

Химические свойства серы
| Реагент | Примеры реакций |
|---|---|
| 1. Взаимодействие с простыми веществами | |
| 1) Неметаллы | Сера вступает в реакции с неметаллами, формируя бинарные соединения, такие как оксиды и галогениды. Если неметалл имеет меньшую электроотрицательность, чем сера, он проявляет положительную степень окисления. Взаимодействие серы с неметаллом, обладающим большей электроотрицательностью, приводит к образованию отрицательной степени окисления. |
| 1) Неметаллы | $S + O_2 = SO_2$ $S + H_2 = H_2S$ $S + 3F_2 = SF_6$ $2S + Cl_2 = S_2Cl_2 \text{ или } SCl_2$ $2S + Br_2 = S_2Br_2 \text{ или } SBr_2$ $S + I_2\not\rightarrow \text{ не взаимодействует}$ $3S + 2P = P_2S_3$ $2S + C = CS_2$ Сероуглерод |
| 2) Металлы | Будучи типичным представителем неметаллов, сера взаимодействует с металлами, образуя бинарные соединения — сульфиды металлов. $S + 2Na t^о→ Na_2S$ $3S + 2Al \xrightarrow{t^\circ} Al_2S_3$ $S + Fe \xrightarrow{t^\circ} FeS$ $S_(нед.) + 2Сu \xrightarrow{t^\circ} Cu_2S$ $S_(изб.) + Сu \xrightarrow{t^\circ} CuS$ $S + Hg \xrightarrow{\text{н.у.}} HgS$ |
| 2. Взаимодействие со сложными веществами | |
| 1) Кислоты-окислители | Сера активно вступает в реакцию с кислотами-окислителями. Так, при действии концентрированной азотной кислоты образуется серная кислота и бурый газ. Реакция с концентрированной серной кислотой протекает по механизму сопропорционирования, приводя к выделению сернистого газа. $S + 6HNO_{3\text{(конц.)}} = H_2SO_4 + 6NO_2 + 2H_2O$ $S + 2H2SO_{4\text{(конц.)}} = 3SO_2 + 2H_2O$ |
| 2) Щёлочи | При нагревании сера растворяется в растворах щелочей, образуя смесь сульфитов и сульфидов: $3S + 6NaOH \xrightarrow{t^\circ} Na_2SO_3 + 2Na_2S + 3H_2O$ |
| 3) Восстановители | При взаимодействии со сложными веществами, выступающими в роли окислителей, сера демонстрирует свойства восстановителя: $3S + 2KClO_3 \xrightarrow{t^\circ} 3SO_2 + 2KCl$ $4S + 3HClO_4 + 4H_2O → 4H_2SO_4 + 3HCl$ $S + K_2Cr_2O_7 \xrightarrow{t^\circ} K_2SO_4 + Cr_2O_3$ |
Соединения серы

Сероводород
Сероводород (H2S) представляет собой бесцветный газ с характерным неприятным запахом протухших яиц, обладающий токсичными свойствами и низкой способностью растворяться в воде. Растворяясь в водной среде, образует слабую сероводородную кислоту.
| Тип реакции | Примеры реакций |
|---|---|
| 1) Кислотно-основные свойства сероводорода | Сероводородная кислота — слабый электролит, кислота-неокислитель. Она вступает в реакцию с активными металлами, соединениями с основными свойствами, а также с солями при условии наличия признаков протекания химической реакции. Взаимодействие солей сильных кислот с сероводородом иногда может носить обратимый характер. $2Na + H_2S = Na_2S + H_2$ $2H_2S + 4Ag + O_2 = 2Ag_2S + 2H_2O$ $Na_2O + H_2S = Na_2S + H_2O$ $2NaOH + H_2S_{\text{(нед.)}} = Na_2S + 2H_2O$ $NaOH + H_2S_{\text{(изб.)}} = NaНS + H_2O$ $ZnSO_4 + H_2S \not\rightarrow$ $FeSO_4 + H_2S \not\rightarrow$ $СuSO_4 + H_2S = CuS\downarrow + H_2SO_4$ $Pb(NO_3)_2 + H_2S = PbS\downarrow + 2HNO_3$ $2AgNO_3 + H_2S = Ag_2S\downarrow + 2HNO_3$ $Na_2[Zn(OH)_4] + 3H_2S_{\text{(изб.)}} = ZnS\downarrow + 2NaHS + 4H_2O$ $Na[Al(OH)_4] + H_2S_{\text{(изб.)}} = Al(OH)3\downarrow + NaHS + H_2O$ |
| 2) Реакции ионного обмена с сульфидами и гидросульфидами | Соли сероводородной кислоты (сульфиды и гидросульфиды) способны вступать в реакции ионного обмена со щелочами, кислотами и другими растворимыми солями при наличии признака реакции. $Na_2S + Sr(OH)_2 = 2NaOH + SrS\downarrow$ $NaНS + NaOH = Na_2S + H_2O$ $Na_2S + ZnCl_2 = ZnS\downarrow + 2NaCl$ $Na_2S + FeCl_2 = FeS\downarrow + 2NaCl$ $Na_2S + CuCl_2 = CuS\downarrow + 2NaCl$ $Na_2S + Pb(NO_3)_2 = PbS\downarrow + 2NaNO_3$ $Na_2S + 2AgNO_3 = Ag_2S\downarrow + 2NaNO_3$ $Na_2S + H_2SO_{4\text{(разб.)}} = Na_2SO_4 + H_2S\uparrow$ $FeS + 2HCl = FeCl_2 + H_2S\uparrow$ $PbS, CuS, Ag_2S, + HCl \not\rightarrow$
$NaНS + HCl = NaCl + H_2S\uparrow$ $Ba(HS)_2 + Na_2SO_4 = BaSO_4\downarrow + 2NaHS$ Сульфиды алюминия ($Al_2S_3$) и хрома ($Cr_2S_3$) невозможно получить в водном растворе вследствие полного необратимого гидролиза. $Al_2S_3 + 6H_2O = 2Al(OH)_3\downarrow + 3H_2S\uparrow$ $Al_2S_3 + 6HCl = 2AlCl_3 + 3H_2S\uparrow$ $Al_2S_3 + 8KOH = 2K[Al(OH)_4] + 3K_2S$ Растворение твёрдого вещества и образование бесцветного раствора. $ 2AlCl_3 + 3Na_2S + 6H_2O = 2Al(OH)_3\downarrow + 3H_2S\uparrow + 6NaCl$ $AlCl_3 + 3NaНS + 3H_2O = Al(OH)_3\downarrow + 3H_2S\uparrow + 3NaCl$ Образуется осадок и выделяется газ с неприятным запахом тухлых яиц. |
| 3) ОВР с сероводородом и его солями | Сероводород и его соли — хорошие восстановители. С конц. кислотами-окислителями и сильными окислителями сера окисляется до максимальной степени окисления: $H_2S + 8HNO_{3\text{(конц.)}} = H_2SO_4 + 8NO_2 + 4H_2O$ $К_2S + 8HNO_{3\text{(конц.)}} = К_2SO_4 + 8NO_2 + 4H_2O$ $Ca(HS)_2 + 16HNO_{3\text{(конц.)}} = CaSO_4 + H_2SO_4 + 16NO_2 + 8H_2O$ $CuS + 8HNO_{3\text{(конц.)}} = CuSO_4 + 8NO_2 + 4H_2O$ $FeS + 12HNO_{3\text{(конц.)}} = Fe(NO_3)_3 + H_2SO_4 + 9NO_2 + 5H_2O$ $FeS_2 + 18HNO_{3\text{(конц.)}} = Fe(NO_3)_3 + 2H_2SO_4 + 15NO_2 + 7H_2O$ C серной кислотой протекает реакция сопропорционирования: $H_2S + 3H_2SO_{4\text{(конц.)}} = 4SO_2 + 4H_2O$ $К_2S + 4H_2SO_{4\text{(конц.)}} = К_2SО_4 + 4SO_2 + 4H_2O$ $CuS + 4H_2SO_{4\text{(конц.)}} = CuSO_4 + 4SO_2 + 4H_2O $ $2FeS + 10H_2SO_{4\text{(конц.)}} = Fe_2(SO_4)_3 + 9SO_2 + 10H_2O$ $2FeS_2 + 14H_2SO_{4\text{(конц.)}} = Fe_2(SO_4)_3 + 15SO_2 + 14H_2O$ Другие ОВР с сероводородом и его солями: $H_2S + 4Cl_2 + 4H_2O = H_2SO_4 + 8HCl$ $H_2S + HClO_4 \rightarrow H_2SO_4 + HCl$ |
| 3) ОВР с сероводородом и его солями | $2Н_2S + O_{2\text{(нед.)}} = 2S + 2Н_2О$ $2Н_2S + 3O_{2\text{(изб.)}} = 2SО_2 + 2Н_2О$ $2CuS + 3O_2 = 2CuO + 2SO_2$ $Ag_2S + O_2 = 2Ag + SO_2$ Слабые окислители, а также окислители-соли, в растворах окисляют сульфид-ион до молекулярной серы: $H_2S + Br_2 = \textcolor{orange}{S\downarrow} + 2НВr$ $H_2S + I_2 = \textcolor{orange}{S\downarrow} + 2НI$ $3К_2S + 8HNO_{3\text{(разб.)}} = 3\textcolor{orange}{S\downarrow}+ 6КNO_3 + 2NO + 4H_2O$ $3H_2S + K_2Cr_2O_7 + 4H_2SO_4 = 3\textcolor{orange}{S\downarrow} + Cr_2(SO_4)_3 + K_2SO_4 + 7Н_2O$ $5K_2S + 2KMnO_4 + 8H_2SO_4 = 3\textcolor{orange}{S\downarrow} + 2MnSO_4 + 6K_2SO_4 + 8Н_2O$ $NaHS + MnO_2 + 3HNO_3 → Mn(NO_3)_2 + \textcolor{orange}{S\downarrow} + NaNO_3 + 2H_2O$ $H_2S + 2FeCl_3 = 2FeCl_2 + \textcolor{orange}{S\downarrow} + 2HCl$ $К_2S_{\text{(нед.)}} + 2FeCl_3 = 2FeCl_2 + \textcolor{orange}{S\downarrow} + 2КCl$ $3К_2S_{\text{(изб.)}} + 2FeCl_3 = 2FeS\downarrow + \textcolor{orange}{S\downarrow} + 6КCl$ $K_2S + 2KNO_2 + 2H_2SO_4 = \textcolor{orange}{S\downarrow}+ 2NO\uparrow + 2K_2SO_4 + 2H_2O$ |
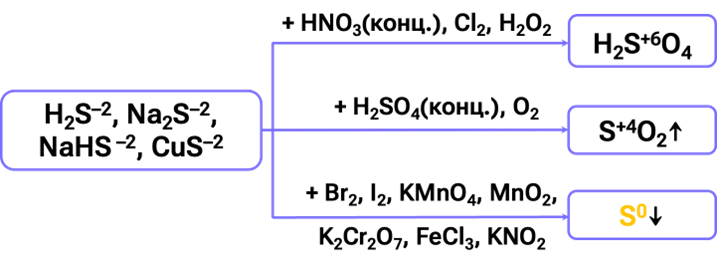
Важно: PbS, CuS, Ag2S подвергаются окислению исключительно концентрированными кислотами-окислителями. Остальные нерастворимые сульфиды металлов способны окисляться различными окислителями в кислой среде. Реакции с образованием оксидов характерны лишь для сульфидов металлов средней активности и неактивных металлов.
Сернистый газ
Сернистый газ (SO2) — бесцветный токсичный газ с резким запахом. Являясь кислотным оксидом, он способен реагировать с водой и с веществами, проявляющими основные свойства, а также вступать в реакции ионного обмена с растворами менее сильных кислот.
| Тип реакции | Примеры реакций |
|---|---|
| 1) Кислотно-основные свойства оксида серы(IV) | Оксид серы(IV) — кислотный оксид, реагирует с веществами, проявляющими основные свойства, с солями более слабых кислот. $SO_2 + H_2O \rightleftarrows H_2SO_3$ $SO_2 + Na_2O = Na_2SO_3$ $SO_2 + 2NaOH_{\text{(избыток)}} = Na_2SO_3 + H_2O$ $SO_2 + NaOH_{\text{(недостаток)}} = NaHSO_3$ $Na_2SiO_3 + 2SO_{2\text{(изб.)}} + 2H_2O = 2NaHSO_3 + Н_2SiO_3\downarrow$ $CaSO_3 + SO_{2\text{(изб.)}} + H_2O = Ca(HSO_3)_2$ |
| 2) Реакции ионного обмена с сульфитами и гидросульфитами | Сульфиты и гидросульфиты — соли, образованные слабой и легколетучей сернистой кислотой. Поэтому они способны вступать в реакции ионного замещения с более сильными кислотами, а также проявлять активность в реакциях с растворами солей. $Na_2SO_3 + 2HCl = 2NaCl + SO_2 + H_2O$ $NaНSO_3 + HCl = NaCl + SO_2 + H_2O$ $Na_2SO_3 + Ba(OH)_2 = 2NaOH + BaSO_3\downarrow$ $2NaНSO_3 + Ba(OH)_ {2\text{(нед.)}} = Na_2SO_3 + BaSO_3\downarrow + 2H_2O$ $NaНSO_3 + Ba(OH)_{2\text{(изб.)}} = NaОН + BaSO_3\downarrow + H_2O$ $Na_2SO_3 + SrCl_2 = SrSO_3\downarrow + 2NaCl$ $2AlCl_3 + 3Na_2SO_3 + 3H_2O = 2Al(OH)_3\downarrow + 3SO_2\uparrow + 6NaCl$ $2NaНSO_3 \xrightarrow{t^\circ} Na_2SO_3 + SO_2 + H_2O$ |
| 3) ОВР с сернистым газом и солями сернистой кислоты | У солей серы (IV) и $SO_2$ наиболее ярко выражены восстановительные свойства, степень окисления серы в таких реакциях повышается до +6: $2SO_2 + O_2 \xrightarrow{кат.} 2SO_3 (кат. — V_2O_5) $ $SO_2 + Br_2 + 2H_2O = H_2SO_4 + 2HBr$ $К_2SO_3 + Br_2 + H_2O = К_2SO_4 + 2HBr$ $К_2SO_3 + Br_2 + 2KOH = К_2SO_4 + 2KBr + Н_2О$ $SO_2 + 2HNO_{3\text{(конц.)}} = H_2SO_4 + 2NO_2$ $К_2SO_3 + 2HNO_{3\text{(конц.)}} = К_2SO_4 + 2NO_2 + Н_2О$ $SO_2 + Н_2O_2 = Н_2SO_4$ $SO_2 + Na_2O_2 = Na_2SO_4$ $SO_2 + Fe_2(SO_4)_3 + 2H_2O = 2FeSO_4 + 2H_2SO_4$ $К_2SO_3 + Fe_2(SO_4)_3 + H_2O = К_2SO_4 + 2FeSO_4 + H_2SO_4$ Это уравнение реакции записывается при протекании реакции и с подкислённым, и с нейтральным раствором перманганата: $5SO_2 + 2KMnO_4 + 2H_2O = 2H_2SO_4 + 2MnSO_4 + K_2SO_4$ Образуется раствор двух солей и кислоты. $5SO_2 + 2HMnO_4 + 2H_2O \rightarrow 2MnSO_4 + 3H_2SO_4$ $5Na_2SO_3 + 2KMnO_4 + 3H_2SO_4 \rightarrow 5Na_2SO_4 + 2MnSO_4 + K_2SO_4 + 3H_2O$ Образуется раствор трёх солей. $3K_2SO_3 + 2KMnO_4 + H_2O \rightarrow 3K_2SO_4 + 2MnO_2\downarrow + 2KOH$ Образуется бурый осадок. $Na_2SO_3 + 2KMnO_4 + 2KOH \rightarrow 2K_2MnO_4 + Na_2SO_4 + H_2O$ Образуется зелёный раствор |
| 3) ОВР с сернистым газом и солями сернистой кислоты | $3SO_2 + K_2Cr_2O_7 + H_2SO_4 \rightarrow K_2SO_4 + Cr_2(SO_4)_3 + H_2O$ Образуется раствор двух солей. $3К_2SO_3 + K_2Cr_2O_7 + 4H_2SO_4 = 4K_2SO_4 + Cr_2(SO_4)_3 + 4H_2O$ Образуется раствор двух солей. $K_2Cr_2O_7 + 3Na_2SO_3 + 4H_2O \rightarrow 2Cr(OH)_3 + 3Na_2SO_4 + 2KOH$ $3Na_2SO_3 + 2CrO_3 + 3H_2SO_4 \rightarrow 3Na_2SO_4 + Cr_2(SO_4)_3 + 3H_2O$ $2KClO_4 + 7Na_2SO_3 + H_2SO_4 \rightarrow Cl_2 + 7Na_2SO_4 + K_2SO_4 + H_2O$ Образуется газ. $2KIO_3 + 5Na_2SO_3 + H_2SO_4 \rightarrow I_2 + 5Na_2SO_4 + K_2SO_4 + H_2O$ Образуется окрашенное простое вещество. $Na_2SO_3 + 3Zn + 8HCl \rightarrow H_2S + 3ZnCl_2 + 2NaCl + 3H_2O$ Образуется газ. $2NaHSO_3 + 6Mg + 7H_2SO_4 \rightarrow Na_2SO_4 + 6MgSO_4 + 2H_2S + 6H_2O$ Образуется газ c неприятным запахом. В присутствии сильных восстановителей $SO_2$ способен проявлять окислительные свойства: $SO_2 + 2C = S + 2CO$ $SO_2 + 2Н_2S = 3S\downarrow + 2H_2O $ $K_2SO_3 + 2K_2S + 6НСl = 3S\downarrow + 6КСl + 3Н_2O$ |
Серный ангидрид
Оксид серы (VI), или серный ангидрид $SO_3$, — в обычных условиях легколетучая бесцветная жидкость с удушливым запахом, кислотный оксид.
| Тип реакции | Примеры реакций |
|---|---|
| 1) Кислотно-основные свойства оксида серы(VI) | Оксид серы(VI) — кислотный оксид, реагирует с веществами, проявляющими основные свойства, с солями более слабых кислот. $SO_3 + H_2O = H_2SO_4$ $SO_3 + K_2O = K_2SO_4$ $3SO_3 + Al_2O_3 = Al_2(SO_4)_3$ $SO_3 + CuO = CuSO_4$ $SO_3 + 2NaOH_{\text{(изб.)}} = Na_2SO_4 + H_2O $ $SO_3 + NaOH_{\text{(нед.)}} = NaHSO_4$ Раствор $SO_3$ в 100%-й серной кислоте называется олеумом. |
Серная кислота
Серная кислота, или гидроксид серы(VI), — сильная двухосновная кислота. Это тяжёлая маслянистая жидкость.
| Тип реакции | Примеры реакций |
|---|---|
| 1) Кислотно-основные свойства оксида серы(VI) | Разбавленная серная кислота обладает всеми свойствами сильных нелетучих кислот (взаимодействует с основными и амфотерными оксидами, с основаниями, амфотерными гидроксидами с образованием соответствующих солей, с металлами, стоящими в ряду напряжений до водорода, вытесняет летучие и более слабые кислоты из их солей:
$H_2SO_{4\text{(разб.)}} + Fe = FeSO_4 + H_2\uparrow$ $H_2SO_4 + CuO = CuSO_4 + H_2O$ $H_2SO_4 + ZnO = ZnSO_4 + H_2O$ $H_2SO_4 + 2NaOH_{\text{(избыток)}} = Na_2SO_4 + 2H_2O$ $H_2SO_{4\text{(избыток)}} + NaOH = NaHSO_4 + H_2O$ $H_2SO_4 + Mg(OH)_2 = MgSO_4 + 2H_2O$ $3H_2SO_4 + 2Al(OH)_3 = Al_2(SO_4)_3 + 6H_2O$ $H_2SO_4 + Na_2CO_3 = Na_2SO_4 + CO_2\uparrow + H_2O$ $H_2SO_4 + Na_2SiO_3 = Na_2SO_4 + H_2SiO_3\downarrow$ |
| 2) Реакции с солями серной кислоты | Растворимые сульфаты вступают в реакции ионного обмена: $Na_2SO_4 + Ba(OH)_2 = BaSO_4\downarrow + 2NaOH$ $CuSO_4 + 2NaOH = Cu(OH)_2\downarrow + Na_2SO_4$ $Na_2SO_4 + BaCl_2 = BaSO_4\downarrow + 2NaCl$
При разложении сульфатов металлов средней активности образуются соответствующие оксиды: $K2SO_4 \xrightarrow{t^\circ} плавится без разложения $2Al_2(SO_4)_3 \xrightarrow{t^\circ} 2Al_2O_3 + 6SO_2 + 3O_2$ $4Fe+2SO_4 \xrightarrow{t^\circ} 2Fe+32O_3 + 4SO_2 + O_2$ $2CuSO_4 \xrightarrow{t^\circ} 2CuO + 2SO_2 + O_2$ $Ag_2SO_4 \xrightarrow{t^\circ} 2Ag + SO_2 + O_2$ |
| 2) Реакции с солями серной кислоты | При прокаливании с углём термически устойчивые сульфаты металлов восстанавливаются до соответствующих сульфидов: $BaSO_4 + 4C \xrightarrow{t^\circ} BaS + 4CO$ $Na_2SO_4 + 4C \xrightarrow{t^\circ} Na_2S + 4CO $ Важно: сульфаты в растворах не проявляют окислительных свойств. Гидросульфаты имеют сильнокислую среду из-за диссоциации: $NaHSO_4 \rightarrow Na^+ + H^+ + SO_4^{\text{2–}}$ $NaHSO_4 + NaOH = Na_2SO_4 + H_2O$ $2NaHSO_4 + Ba(OH)_ {2\text{(нед.)}} = Na_2SO_4 + BaSO_4\downarrow + 2H_2O$ $NaHSO_4 + Ba(OH)_ {2\text{(изб.)}} = NaОН + BaSO_4\downarrow + H_2O$ $NaHSO_4 + СН_3СООNa \rightarrow Na_2SO_4 + CH_3COOH$ $NaHSO_4 + Ba(NO_3)_2 \rightarrow BaSO_4\downarrow + NaNO_3 + HNO_3$ $NaHSO_4 + (СН_3СОО)_2Ba_{\text{(изб.)}} \rightarrow \\ BaSO_4\downarrow + CH_3COOH + CH_3COONa$ $2NaHSO_4 + Fe \rightarrow Na_2SO_4 + FeSO_4 + H_2\uparrow$ |
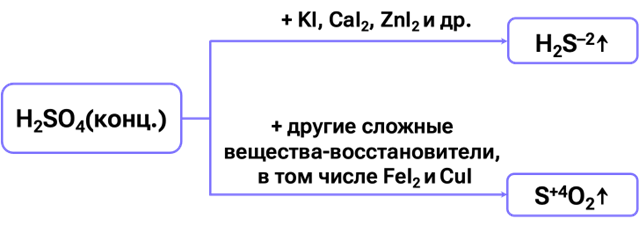
| 3) ОВР с простыми веществами | Концентрированная серная кислота проявляет свойства сильного окислителя и является кислотой-окислителем. Может реагировать как с металлами (в том числе стоящими после водорода), так и с некоторыми неметаллами. Взаимодействие концентрированной серной кислоты с металлами Схема реакции: $Me + H_2SO_{4\text{(конц.)}} = {\text{сульфат металла в высшей степени \\ окисления + продукт восстановления серы}} + Н_2О$ $2H_2SO_{4\text{(конц.)}} + Cu = CuSO_4 + SO_2\uparrow + 2H_2O $ $2H_2SO_{4\text{(конц.)}} + 2Ag = Ag_2SO_4 + SO_2\uparrow + 2H_2O$ $6H_2SO_{4\text{(конц.)}} + 2Fe \xrightarrow{t^\circ} Fe2(SO_4)_3 + 3SO_2\uparrow + 6H_2O$ $6H_2SO_{4\text{(конц.)}} + 2Al \xrightarrow{t^\circ} Al_2(SO_4)_3 + 3SO_2\uparrow + 6H_2O$ $Zn + 2H_2SO_{4\text{(конц.)}} = ZnSO_4 + SO_2\uparrow + 2H_2O$ $5H_2SO_{4\text{(конц.)}} + 4Mg = 4MgSO_4 + H_2S\uparrow + 4H_2O$ Взаимодействие концентрированной серной кислоты с неметаллами Схема реакции: $H_2SO_{4\text{(конц.)}} + неМе = {\text{кислота неМе \\ в высшей степени окисления}} + SO_2 + H_2O$ $2P + 5H_2SO_{4\text{(конц.)}} = 2H_3PO_4 + 5SO_2 + 2H_2O$ $С + 2H_2SO_{4\text{(конц.)}} = CO_2+ 2SO_2 + 2H_2O$ $S + 2H_2SO_{4\text{(конц.)}} = 3SO_2+ 2H_2O$ $I2 + H_2SO_{4\text{(конц.)}} \not\rightarrow$ |
| 4) ОВР со сложными веществами | Концентрированная серная кислота демонстрирует выраженные окислительные свойства не только при реакциях с простыми веществами, но и при взаимодействии со сложными соединениями. Степень восстановления серы зависит от силы применённого восстановителя. $H_2SO_{4\text{(конц.)}} + NaCl_{\text{(тв.)}} = NaHSO_4 + HCl\uparrow$ $3H_2SO_{4\text{(конц.)}} + 2KBr = Br_2 + SO_2\uparrow + 2KHSO_4 + 2H_2O$ $5H_2SO_{4\text{(конц.)}} + 8KI = 4I_2 + H_2S\uparrow + 4K_2SO_4 + 4H_2O$ $6H_2SO_{4\text{(конц.)}} + 2FeI_2 = Fe_2(SO_4)_3 + 2I_2 + 3SO_2\uparrow + 6H_2O$ $2CrCl_2 + 4H_2SO_{4\text{(конц.)}} → Cr_2(SO_4)_3 + \\ SO_2\uparrow + 4HCl\uparrow + 2H_2O$ $PH_3 + 4H_2SO_{4\text{(конц.)}} = H_3PO_4 + 4SO_2 + 4H_2O$ $2FeO + 4H_2SO_{4\text{(конц.)}} = Fe_2(SO_4)_3 + SO_2 + 4H_2O$ $Fe_3O_4, Fe(OH)_2, \text{cоли железа} (II) + H_2SO_{4\text{(конц.)}} \rightarrow Fe_2(SO_4)_3 + SO_2 + H_2O$ $Cu_2O + 3H_2SO_{4\text{(конц.)}} = 2CuSO_4 + SO_2 + 3H_2O$ |
Обобщение ОВР с концентрированной серной кислотой и металлами
| Продукт восстановления серы | Активность металла |
|---|---|
| SO2↑ бесцветный газ с резким запахом | Неактивные металлы (Pb, Сu, Ag, Hg) и Al, Cr, Fe, которые пассивируются кислотой при н. у., реакция протекает только при нагревании |
| S↓ жёлтое твёрдое простое вещество | Металлы средней активности (Zn)* |
| H2S↑ бесцветный газ с неприятным запахом тухлых яиц | Активные металлы (ЩМ, ЩЗМ, Mg) |
| Au, Pt, Pd реагируют только с царской водкой и не реагируют с серной кислотой конц. | |
Обобщение ОВР с концентрированной серной кислотой и сложными веществами
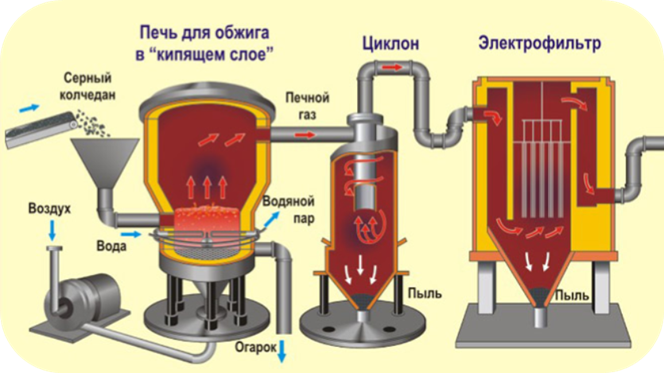
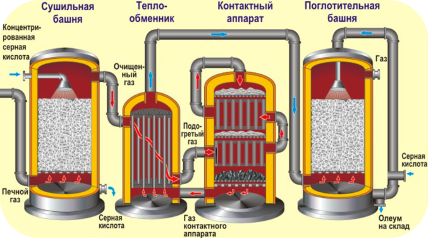
Промышленное получение серной кислоты
| Стадия | Процесс |
|---|---|
| I стадия | Обжиг пирита $FeS_2$ в печи для обжига в кипящем слое: $4FeS_2 + 11O_2 = 2Fe_2O_3 + 8SO_2 + Q$ (t = 800 оC) Принцип «кипящего слоя» |
| II стадия | Окисление $SO_2$ в $SO_3$ кислородом Процесс протекает в контактном аппарате в соответствии с уравнением реакции: $2SO_{2\text{(г.)}} + O_{2\text{(г.)}} \rightleftarrows 2SO_{3\text{(г.)}} + Q$ В контактном аппарате |
| III стадия | Поглощение $SO_3$ серной кислотой. $nSO_3 + H_2SO_4 = H_2SO_4 \times nSO_3 (олеум) $ В поглотительной башне |
Способы получения серы
Промышленные способы.
В промышленности серу выплавляют из ископаемой самородной серы.
Промышленные способы.
В лаборатории для получения серы используют неполное окисление сероводорода:
$2H_2S + O_{2\text{(нед.)}} = 2S + 2H_2O$
$2H_2S + SO_2 = 3S + 2H_2O$
Применение некоторых соединений
| Формула вещества | Тривиальные/ систематические названия вещества | Область применения |
|---|---|---|
| S | Сера | Получения оксида серы(IV), серной кислоты, сероуглерода $CS_2$; для вулканизации резины; в производстве пороха |
| $CS_2$ | Сероуглерод или сульфид углерода(IV) | Растворитель |
| $FeS_2$ | Дисульфид железа(II) или пирит | Получение серной кислоты |
| $SO_2$ | Оксид серы(IV) или сернистый газ | В пищевой промышленности используется как консервирующее и антибактериальное вещество |
| $Н_2SO_4$ | Серная кислота | Серная кислота широко используется в химической промышленности для производства синтетических моющих средств, пластмасс, удобрений и лекарственных препаратов, также это водоотнимающее средство |
| $CaSO_4\times 2H_2O$ | Дигидрат сульфата кальция или гипс | Строительный материал |
Заключение
Изучив свойства серы и её соединений, можно сделать важный вывод: сера образует разнообразные вещества, и каждое из них имеет свои особенности. Эти соединения по-разному проявляют себя в химических реакциях и отличаются физическими свойствами. Понимание этих закономерностей помогает лучше разобраться в химических процессах и уверенно применять знания на практике.
Автор:
Рогова Любовь, методист «100балльного репетитора» по химии ЕГЭ