Введение
Открытие Периодического закона Дмитрием Ивановичем Менделеевым в 1869 году стало поворотным моментом в развитии химической науки, преобразовав разрозненные эмпирические знания о химических элементах в целостную систему. Созданная на его основе Периодическая система стала не просто удобной таблицей для классификации, а мощным инструментом научного предвидения, позволившим предсказать существование и характеристики новых элементов задолго до их экспериментального обнаружения.
В рамках статьи узнаем:
- ценность и фундаментальные следствия из Периодического закона Д. И. Менделеева
- устройство Периодической системы химических элементов
- свойства химических элементов, которые изменяются периодически
Как появились периодический закон и Периодическая система химических элементов Дмитрия Ивановича Менделеева?
С древних времён и по сегодняшний день люди открывают новые элементы, и в какой-то момент этих элементов стало так много, что появилась необходимость в их систематизации. Учёные-химики из разных стран пытались создать свою собственную периодическую систему и свой собственный периодический закон, но больше всех преуспел Д. И. Менделеев, и это одно из самых величайших открытий человечества.
Почему? Потому что Д. И. Менделеев расположил химические элементы таким образом, что в дальнейшем, когда произошли открытия в строении атома (например, открытие электрона), оказалось, что те концепции, которые он заложил в свою систему, верны.
Интересно, что сама идея периодичности вызревала в научной среде задолго до Менделеева. Немецкий химик Иоганн Вольфганг Дёберейнер ещё в 1829 году заметил, что атомный вес стронция близок к среднему арифметическому атомных весов кальция и бария. Позже француз де Шанкуртуа расположил элементы на винтовой линии, а англичанин Ньюлендс сформулировал «закон октав». Однако именно Менделееву удалось увидеть за отдельными закономерностями единый принцип.
Отличительной чертой Периодической системы, подтверждающей её научную значимость, является способность к прогнозированию. При создании таблицы Менделеев преднамеренно оставил незаполненные позиции для элементов, существование которых он теоретически обосновал, но которые ещё не были обнаружены экспериментально. Удивительная точность его предсказаний впоследствии подтвердилась при открытии таких элементов, как галлий Ga, скандий Sc и германий Ge, свойства которых учёный описал задолго до их обнаружения.
Это уникальное изобретение — ваша официальная шпаргалка на ЕГЭ, это то, что вам в течение этого учебного года будет очень сильно помогать в решении заданий и, конечно же, в понимании химии.
Вот так сформулировал свой закон Дмитрий Иванович Менделеев:

А вот так периодический закон звучит сейчас:


Как устроена Периодическая система химических элементов Д. И. Менделеева?
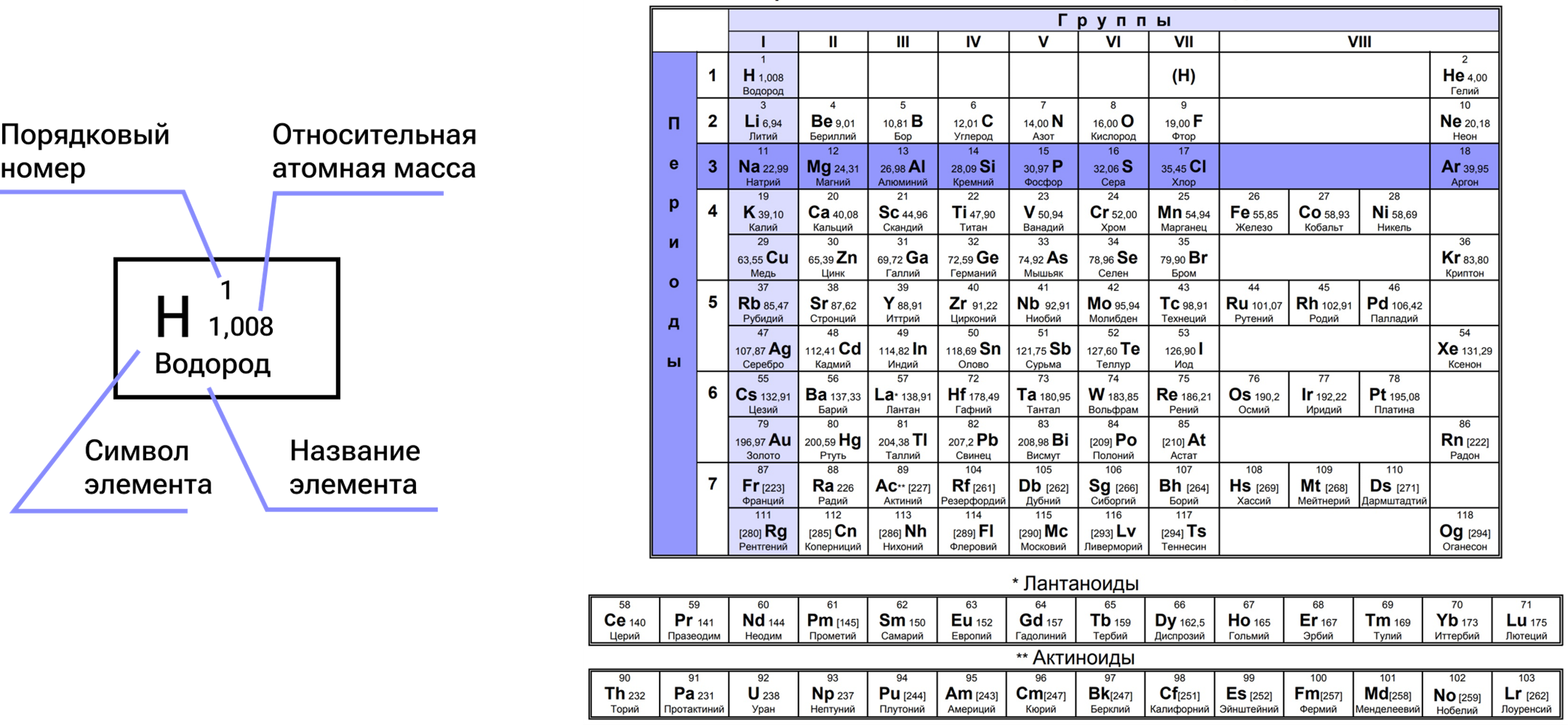
Период — горизонтальный ряд Периодической системы химических элементов, последовательность атомов по возрастанию заряда ядра и заполнению электронами внешней электронной оболочки.
Первый период, содержащий 2 элемента, а также второй и третий, содержащие по 8 элементов, называются малыми.
Остальные периоды, имеющие 18 и более элементов, — большими.
Группа — вертикальный столбец Периодической системы химических элементов, последовательность атомов по возрастанию заряда ядра, обладающих однотипным электронным строением.
Каждая группа состоит из главной (А) и побочной (В) подгрупп.
Элементы главных подгрупп имеют валентные s- и p-электроны. Элементы побочных подгрупп (переходные элементы) имеют валентные d- и f-электроны.
Все элементы побочных подгрупп — металлы.
Как ещё можно для себя запомнить, где в таблице, используемой на ЕГЭ, расположены элементы главных и побочных подгрупп?
Элементы малых периодов (периоды 1–3) являются элементами главных подгрупп, а значит все те элементы, которые расположены под ними являются элементами главных подгрупп.
В качестве примера можно рассмотреть V группу: элемент второго периода — азот N определяет принадлежность к главной подгруппе таких элементов, как фосфор P, мышьяк As, сурьма Sb и висмут Bi. В эту же группу входят элементы побочной подгруппы — ванадий V, ниобий Nb и тантал Ta, относящиеся к переходным металлам.
Характерной чертой элементов, составляющих главную подгруппу, является сходство электронных конфигураций внешнего энергетического уровня, описываемых общей формулой.
Проиллюстрируем это на примере элементов IIIА группы: бора B, алюминия Al, галлия Ga, индия In и таллия Tl.
В своих периодах они следуют за элементами IА и IIА групп, у которых заполняется s-подуровень. Раз это элементы главной подгруппы, то у каждого из них заполняется идущий за s-подуровнем — p-подуровень, на который добавляется 1 электрон. Конфигурации внешнего энергетического уровня:
B — 2s²2p¹, Al — 3s²3p¹, Ga — 4s²4p¹, In — 5s²5p¹, Tl — 6s²6p¹.
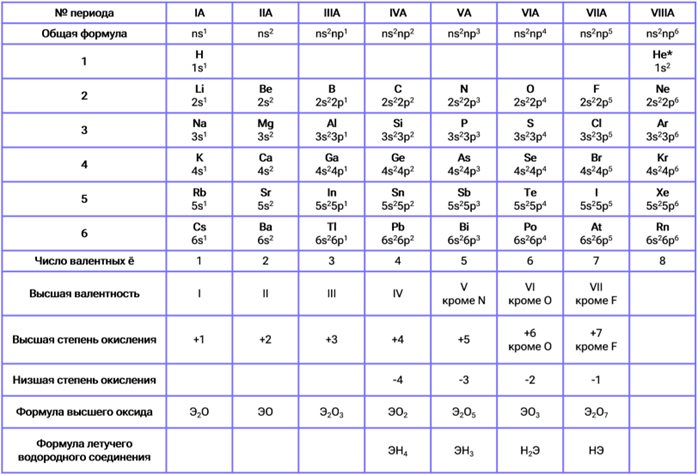
Элементы, относящиеся к одной главной подгруппе, демонстрируют единообразие в строении внешнего электронного слоя, которое выражается общей формулой ns²np¹. Параметр n в данной формуле отображает главное квантовое число, совпадающее с номером периода. Сумма электронов на внешних подуровнях (s² + p¹ = 3) находится в строгом соответствии с номером группы (III), что подтверждает системный характер Периодического закона.
Для элементов других групп главных подгрупп общие электронные конфигурации составляются аналогично:
Рассмотрим элементы побочных подгрупп, например, IIIВ группы, так как именно в этой группе расположен первый d-элемент — скандий Sc. Согласно порядку заполнения орбиталей электронами после 4s-подуровня заполняется 3d-подуровень. Электронная конфигурация валентных электронов скандия — 3d¹4s².
Следующий элемент, титан Ti, имеет конфигурацию 3d²4s². Далее заполнение d-орбиталей в четвёртом периоде происходит закономерно, за исключением двух элементов — хрома Cr и меди Cu. Ожидая конфигурации Cr — 3d⁴4s² и Cu — 3d⁹4s², стоит вспомнить о явлении проскока (перескока или провала) электрона, связанного с наиболее выгодными состояниями наполовину или полностью заполненного электронного подуровня (подробнее ты можешь узнать об этом в статье «Электронные и электронно-графические формулы атомов и ионов»).
Таким образом, для элементов IB и VIB групп четвёртого периода конфигурации валентных электронов принимают вид 3d⁵4s¹ для хрома и 3d¹⁰4s¹ для меди. Электронные конфигурации элементов одной группы побочной подгруппы также схожи.
Электронные конфигурации элементов одной группы побочной подгруппы:
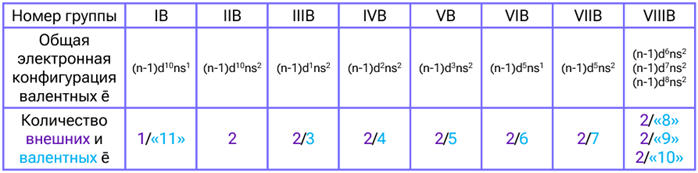
Для переходных элементов понятия «внешние» и «валентные» электроны различны. Внешними для них являются электроны на s-подуровне, следующем за предвнешним d-подуровнем. Валентными же являются как s-, так и d-электроны. Кроме того, важно отметить, что общее количество валентных электронов не всегда равно максимальной валентности элемента (в таблице это обозначено «»).
Современная таблица содержит несколько «неудобных» мест, бросающих вызов стройной системе. Водород, например, располагается одновременно в 1 и 7 группе — он может как отдавать электрон, подобно щелочным металлам, так и принимать, подобно галогенам. Лантаноиды и актиноиды, «вынесенные» за пределы основной таблицы, напоминают нам, что природа сложнее любой классификации. А недавно синтезированные сверхтяжёлые элементы живут доли секунды, но всё же подчиняются периодическому закону.
Какую ещё информацию мы можем извлечь из периодического закона Д. И. Менделеева?
Периодичность — это повторяемость химических и некоторых физических свойств у простых веществ и соединений при изменении порядкового номера элемента при переходе от периода к периоду.
Какие свойства элементов главных подгрупп меняются периодически?
- Число валентных электронов.
- Радиус атома.
- Электроотрицательность.
- Окислительные (неметаллические)/восстановительные (металлические) свойства.
- Кислотные/основные свойства оксидов и гидроксидов
- Кислотные/основные свойства летучих водородных соединений
Давайте посмотрим на них повнимательнее.
1. Число валентных электронов
От элемента к элементу увеличению заряда ядра атома сопутствует нарастание общего числа электронов и периодически повторяющиеся изменения в организации валентных электронных оболочек. Именно эта периодичность в изменении электронной конфигурации внешних уровней определяет характер изменения физико-химических свойств элементов, их соединений и лежит в основе систематизации элементов.
2. Радиус атома
Рост номера периода сопровождается увеличением количества энергетических уровней в атомах, что вызывает закономерное возрастание атомного радиуса. Таким образом, при движении вниз по группе атомный радиус увеличивается. Эта тенденция проявляется при движении сверху вниз по любой группе Периодической системы.
В пределах одного периода при последовательном переходе от элемента к элементу наблюдается увеличение числа внешних электронов и заряда ядра при сохранении постоянного количества энергетических уровней. Это неизбежно влечёт за собой усиление электростатического (кулоновского) притяжения между ядром и электронной оболочкой, вследствие чего при движении по периоду слева направо атомный радиус уменьшается.
Самые маленькие радиусы среди всех элементов — у водорода и гелия.
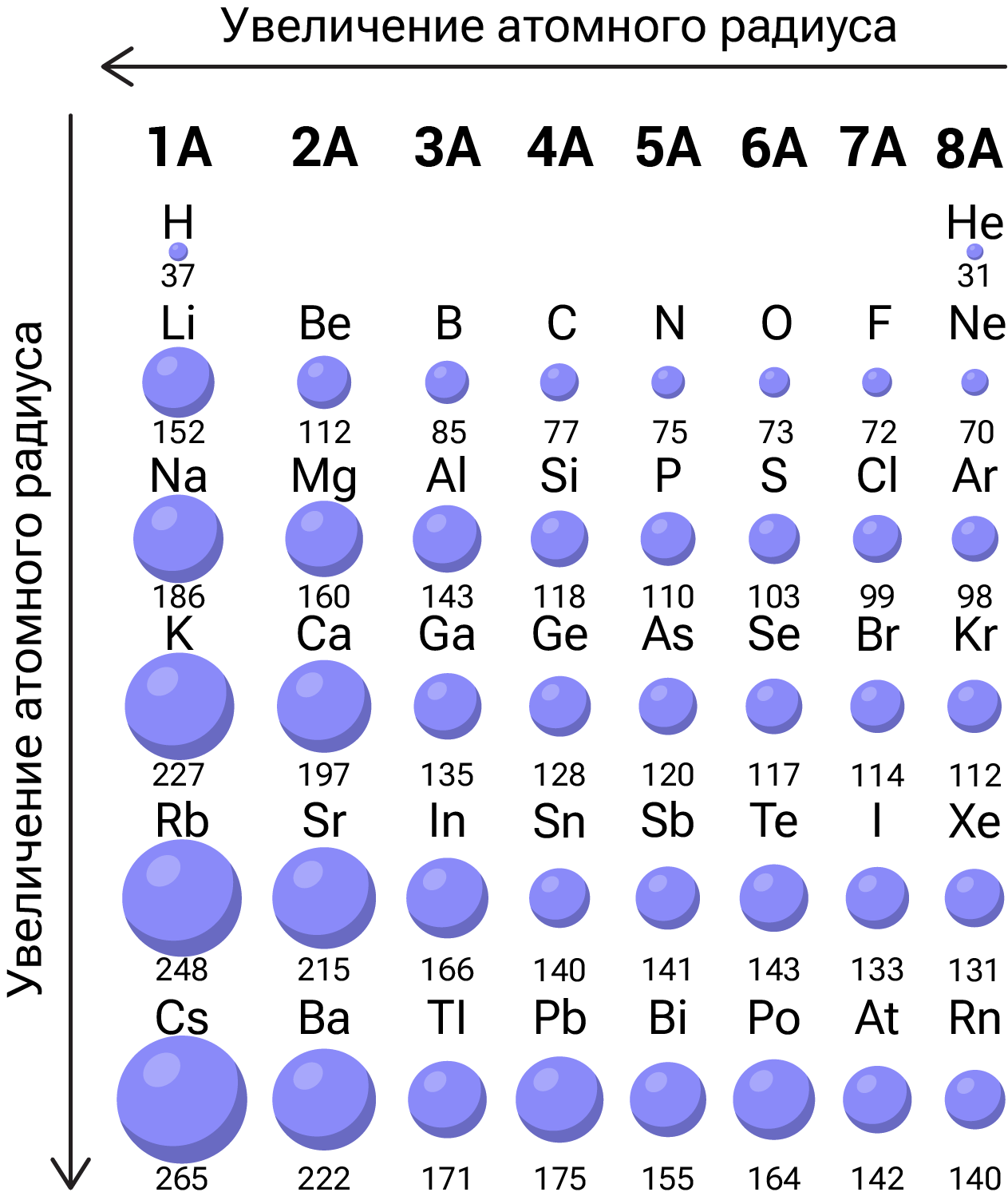

Рассмотрим задачу на расположение элементов кислорода O, кремния Si и фтора F в порядке уменьшения атомного радиуса. Согласно периодическому закону, кремний, находящийся в третьем периоде, имеет больший радиус по сравнению с элементами второго периода (O и F), поскольку у атома кремния на один энергетический уровень больше. Сравнивая кислород и фтор в пределах второго периода, учитываем уменьшение радиуса элементов при движении по периоду слева направо. Правильный порядок расположения элементов: Si → O → F.
3. Электроотрицательность
Электроотрицательность — способность атома притягивать к себе электроны другого атома.
Атомы с высокой электроотрицательностью принимают/притягивают электроны, как правило, это неметаллы; атомы, легко отдающие свои электроны, обладают низкими значениями электроотрицательности, в основном — это металлы.
Значение электроотрицательности зависит от соотношения радиуса атома и количества внешних электронов.
Исходя из этого, можно обозначить два ориентира в Периодической системе:
→ Фтор F обладает довольно маленьким радиусом атома и имеет 7 внешних электронов, которые испытывает мощное притяжение со стороны атомного ядра. Кроме того этот элемент VIIА группы стремится присоединить один электрон для формирования стабильной электронной оболочки инертного газа. Уникальная комбинация свойств определяет фтор как самый электроотрицательный элемент в Периодической системе.
→ Франций Fr имеет очень большой радиус, а на внешнем энергетическом уровне всего один электрон, который очень слабо притягивается к положительному ядру атома и его просто оторвать. Франций — элемент с самой низкой электроотрицательностью.
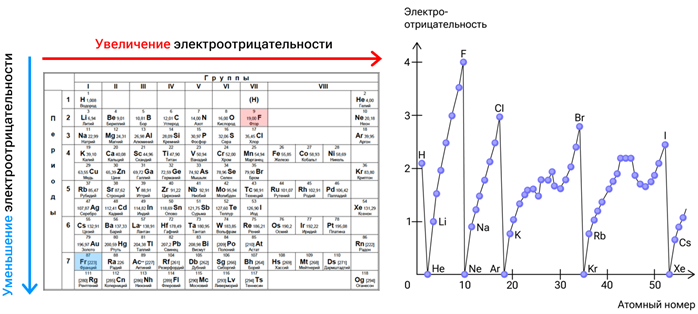
Таким образом, электроотрицательность увеличивается при движении по периоду — слева направо, при движении по группе — снизу вверх, то есть от франция ко фтору.
4. Металлические и неметаллические свойства
Металлические свойства характеризуются способностью атомов химического элемента отдавать электроны, то есть проявлять восстановительные свойства.
Неметаллические свойства характеризуются способностью атомов химического элемента присоединять электроны, то есть проявлять окислительные свойства.
Существует чёткая взаимосвязь между электроотрицательностью и проявлением металлических/неметаллических свойств.
Низкие значения электроотрицательности обусловливают металлические свойства элементов, выражающиеся в способности атомов отдавать электроны, в то время как высокая электроотрицательность характерна для атомов элементов, проявляющих неметаллические свойства, то есть склонных притягивать электроны.
Условная линия, соединяющая бор B и астат At, разделяет Периодическую систему на две характерные области: металлы и неметаллы. Элементы главных подгрупп, находящиеся выше данной линии, проявляют типичные неметаллические свойства, тогда как расположенные ниже относятся к металлам. Важно отметить, что все переходные элементы, составляющие побочные подгруппы, как уже было сказано ранее, по своей природе являются металлами.
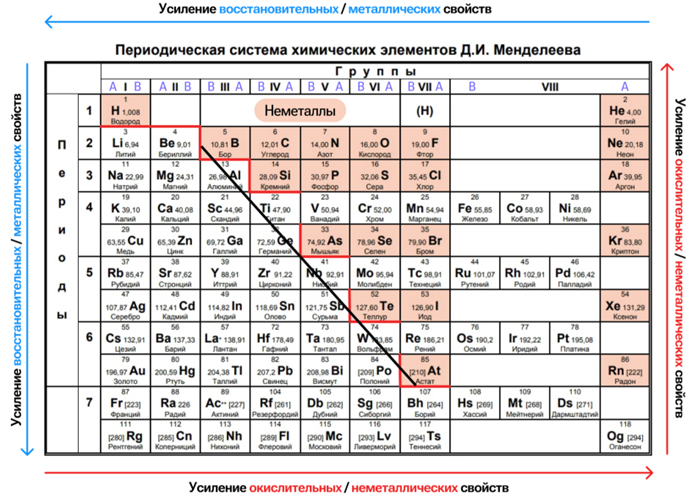
Тенденции в изменении неметаллических свойств и окислительной способности элементов полностью соответствуют изменению электроотрицательности. При движении вниз по группе неметаллические свойства и окислительная способность ослабевают вместе с уменьшением электроотрицательности, а металлические свойства и восстановительная способность элементов возрастают. При движении по периоду слева направо неметаллические свойства и окислительная способность усиливаются, а металлические свойства и восстановительная способность ослабевают.
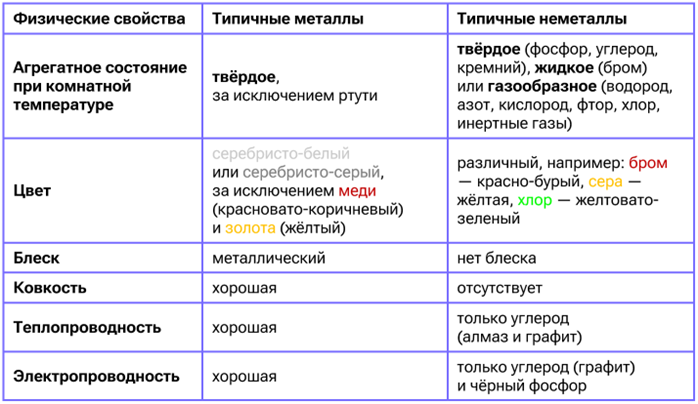
Деление элементов на металлы и неметаллы происходит не только на основе диагонали В-At (5-85 или «ступеньки») в Периодической системе, но в большей степени на основе физических и химических свойств.
В силу схожести свойств элементов одной группы одной подгруппы выделяют группы химических элементов:
- Щелочные металлы — металлы первой группы главной подгруппы: Li, Na, K, Rb, Cs, Fr.
- Щелочноземельные металлы — металлы второй группы главной подгруппы: Ca, Sr, Ba, Ra.
- Пниктогены — элементы пятой группы главной подгруппы: N, P, As, Sb, Bi, Mc.
- Халькогены — элементы шестой группы главной подгруппы: O, S, Se, Te, Po, Lv.
- Галогены — элементы седьмой группы главной подгруппы: F, Cl, Br, I, At, Ts.
- Инертные газы (благородные газы)— элементы восьмой группы главной подгруппы: He, Ne, Ar, Kr, Xe, Rn, Og.
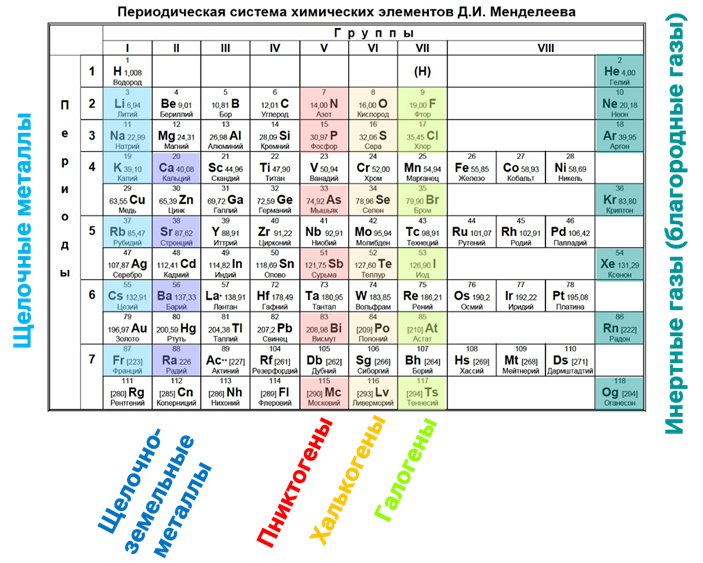
5. Кислотно-основные свойства оксидов и гидроксидов
Металлам (в низкой степени окисления) соответствуют основные оксиды и основания (основные гидроксиды).
Неметаллам — кислотные оксиды и кислоты (кислотные гидроксиды).
Основность оксидов и гидроксидов находится в прямой зависимости от интенсивности металлических свойств элемента: чем более ярко выражен металлический характер, тем сильнее основные свойства этих соединений. Схожая зависимость проявляется для неметаллов — усиление их характерных свойств приводит к возрастанию кислотности образуемых ими оксидов и гидроксидов.
Кислотно-основной характер соединений элементов подчиняется строгой периодичности, аналогичной изменению металлических и неметаллических свойств. Диагональ B-At служит не только разделительной линией между металлами и неметаллами, но и маркером для классификации их соединений: ниже диагонали преобладают основные оксиды и гидроксиды, выше — кислотные. Особую группу образуют элементы, такие как бериллий, алюминий, олово, свинец и др., расположенные в непосредственной близости от этой условной границы — образуемые ими соединения проявляют амфотерные (двоякие) свойства.
При движении вниз по группе фиксируется усиление основных и ослабление кислотных свойств оксидов и гидроксидов. В направлении слева направо по периоду, напротив, отмечается усиление кислотных и ослабление основных свойств. Данная периодическая зависимость просматривается и в структуре периодов: период открывает типичный металл, образующий основные соединения, тогда как окончание периода представлено неметаллом, образующим кислотные оксиды и кислоты.
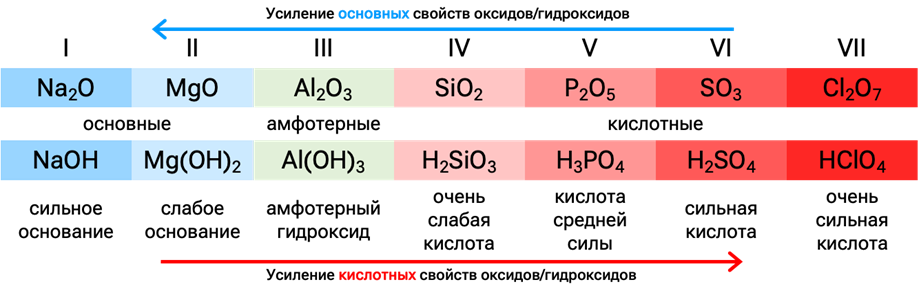
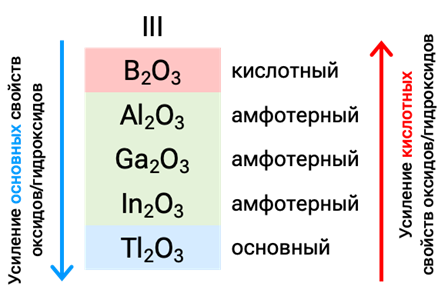
6. Кислотно-основные свойства летучих водородных соединений
Способностью образовывать летучие водородные соединения обладают только типичные элементы-неметаллы.
Летучие водородные соединения неметаллов второго периода демонстрируют различную химическую природу: метан (CH₄) — не обладает кислотными или основными свойствами, аммиак (NH₃) — проявляет слабые основные свойства (в растворе), вода (H₂O) — амфотерное соединение, фтороводород (HF) — слабая кислота (в растворе).
В пределах периода слева направо наблюдается закономерное усиление кислотных свойств водородных соединений, соответствующее возрастанию неметаллических свойств элементов.
При движении вниз по группе кислотные свойства усиливаются вследствие увеличения длины связи H-Э и уменьшения её прочности, что облегчает диссоциацию.
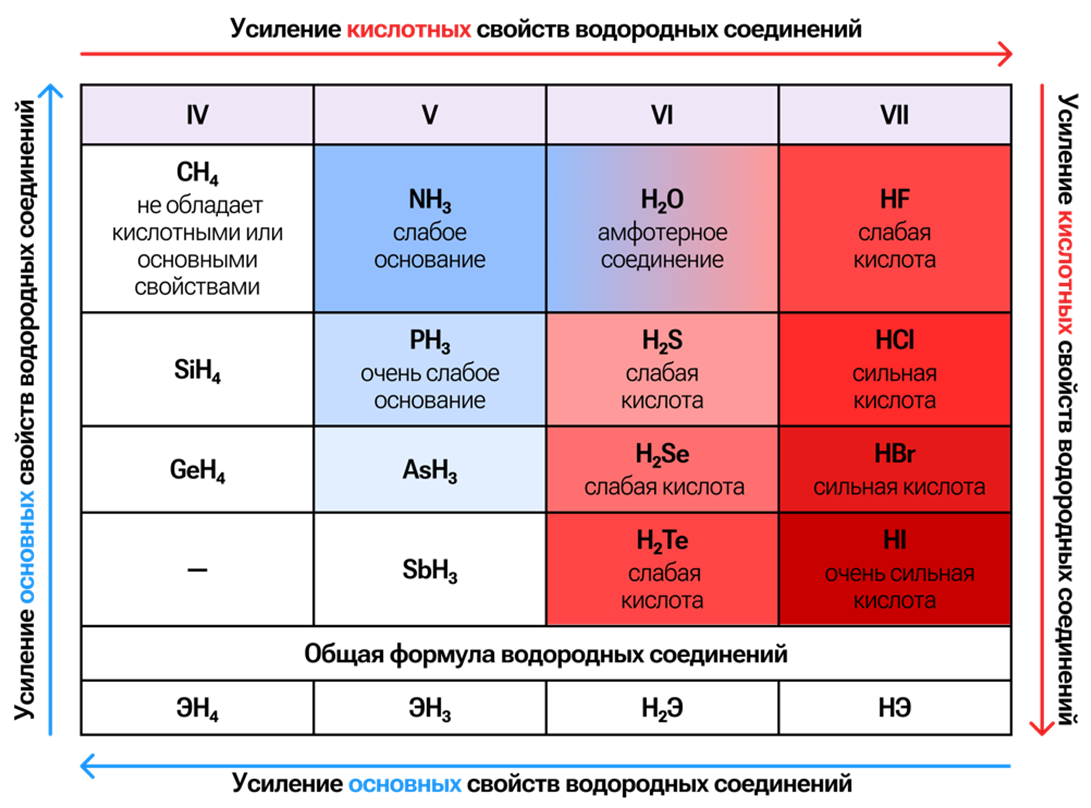
Обобщим рассмотренные выше металлические/неметаллические и основные/кислотные свойства:
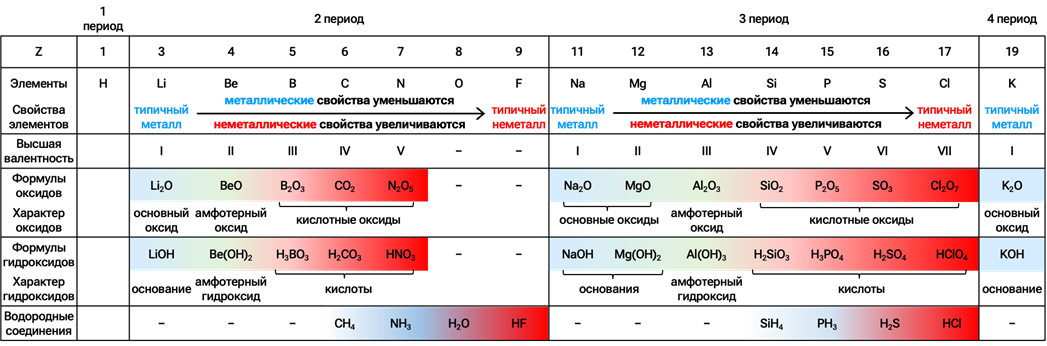
В варианте Периодической системы Д. И. Менделеева, использующейся на ЕГЭ, удобно определить две основные тенденции: движение ко фтору и движение ко францию.

Периодическое изменение свойств элементов и сложных соединений, которые они образуют
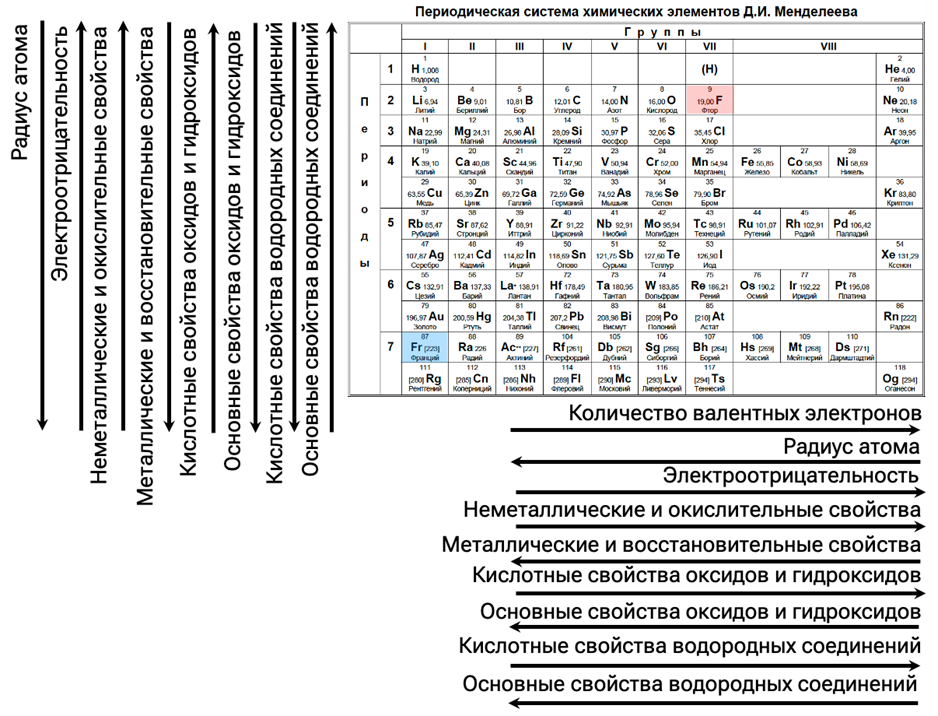
Периодический характер изменения свойств элементов и их соединений, подробно проанализированный выше, создает целостную картину химического поведения веществ. Кроме того, знание Периодического закона пригодится вам при решении задания № 2 ЕГЭ.
Заключение
Периодический закон демонстрирует единство материального мира. Химические свойства элементов оказываются связанными с фундаментальными физическими константами — зарядом ядра, радиусом атома, энергиями отрыва и присоединения электронов. Эта взаимосвязь проявляется даже в биологии: состав живых организмов преимущественно включает элементы второго и третьего периодов, что не случайно — именно эти элементы обладают оптимальным балансом между стабильностью и реакционной способностью для построения сложных молекулярных систем.
Периодический закон прошёл проверку временем, превратившись из эмпирического правила в фундаментальный закон природы. Современная Периодическая система насчитывает уже 118 химических элементов, а периодический закон продолжает служить ориентиром для учёных современности.
Автор:
Щерба Тарас, методист «100балльного репетитора» по химии ЕГЭ