Введение
В начале XIX века учёные задумались о том, как устроен атом. В 1808 году Джон Дальтон предложил сферическую модель атома. Её суть заключалась в том, что атом — сфера, внутри которой находится что-либо.

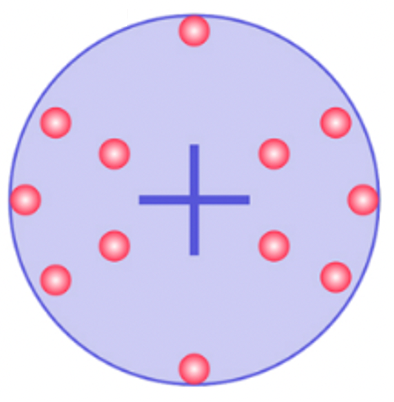
Джозеф Джон Томсон в 1904 году предложил пудинговую модель атома (булочка с изюмом). Она подразумевала, что весь объем атома (булочка) заряжен положительно, а отрицательные частицы вставлены в него как изюм. В этой модели атом является электронейтральным.
Планетарная модель
В 1911 году Эрнест Резерфорд провёл опыт по рассеянию альфа-частиц в тонкой золотой фольге. На основании результатов эксперимента, была предложена планетарная модель атома.
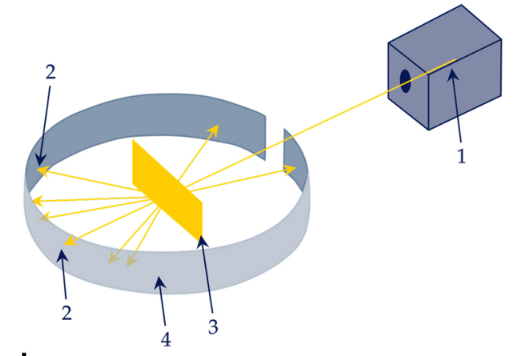
Где:
- источник альфа-частиц;
- траектории движения альфа-частиц после прохождения через тонкую золотую фольгу;
- тонкая золотая фольга;
- экран, покрытый сернистым цинком.
После пролёта через золотую фольгу альфа-частицы двигаются по разным траекториям. Резерфорд предположил, что при движении внутри фольги некоторые частицы сталкиваются с атомами золота и изменяют свою траекторию. Другие частицы пролетают между атомами, поэтому двигаются прямолинейно. Это возможно только в случае, если ядро атома будет значительно меньше размеров самого атома золота.
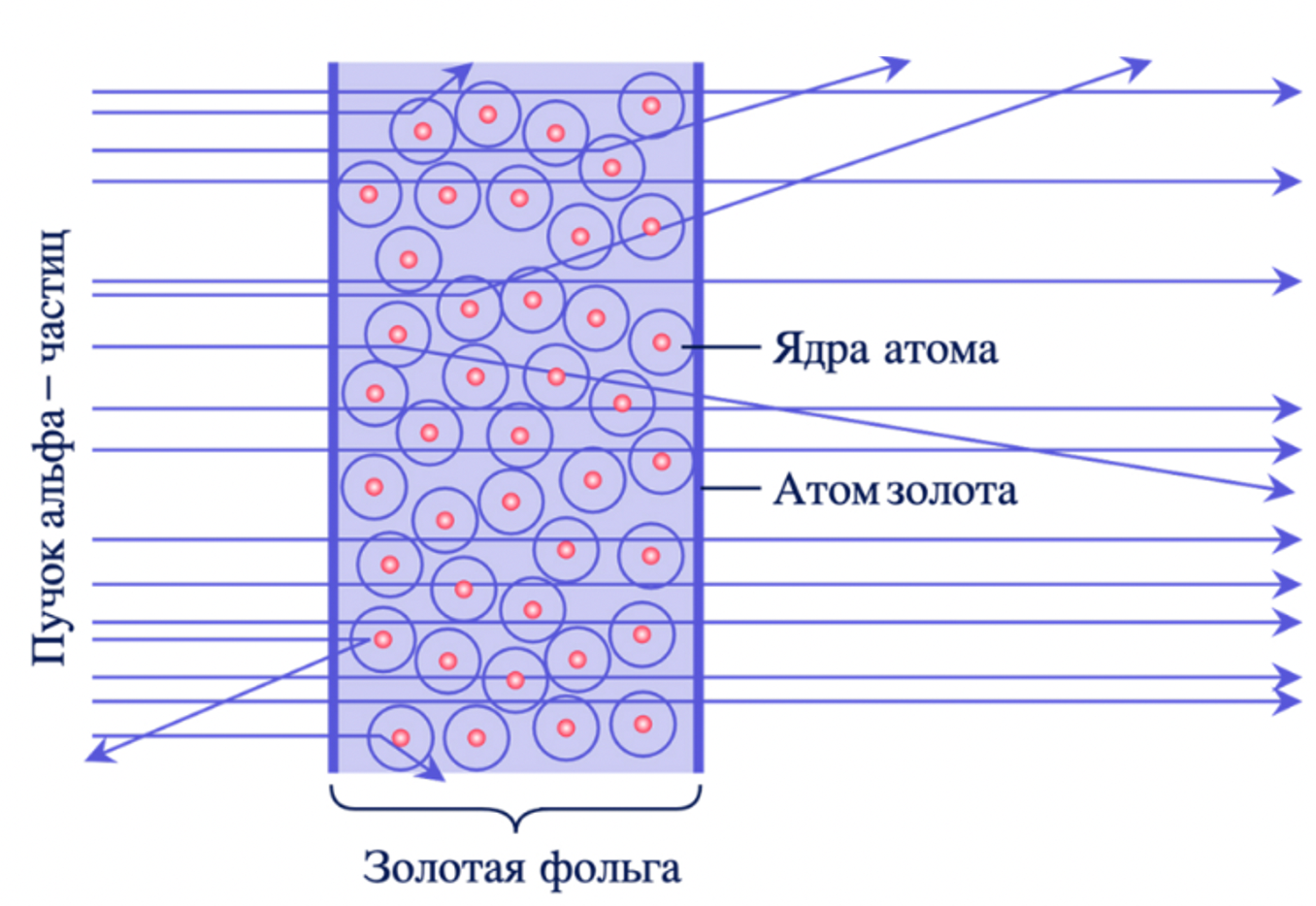
На основании этого опыта, Резерфорд предложил новую модель строения атома.
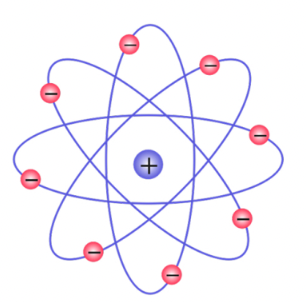
В модели Резерфорда атом имеет положительно заряженное ядро, вокруг которого по орбитам вращаются отрицательно заряженные электроны.
Проблема этой модели заключалась в том, что электроны, вращаясь вокруг ядра, будут являться источниками электромагнитных волн, а значит будут терять энергию. В результате этого радиус их орбит должен постепенно уменьшаться, что в итоге приведёт к аннигиляции электрона положительным зарядом. Однако в действительности этого не наблюдалось.

Квантовая модель Бора
В 1913 году Нильс Бор решил проблему модели Резерфорда, предложив квантовую модель строения атома. Согласно модели атома Бора, электроны вращаются вокруг положительно заряженного ядра по стационарным орбитам. Причём находясь на этих орбитах, атом не излучает и не поглощает энергию. При переходе с одной орбиты на другую электрон будет излучать или поглощать электромагнитную волну.
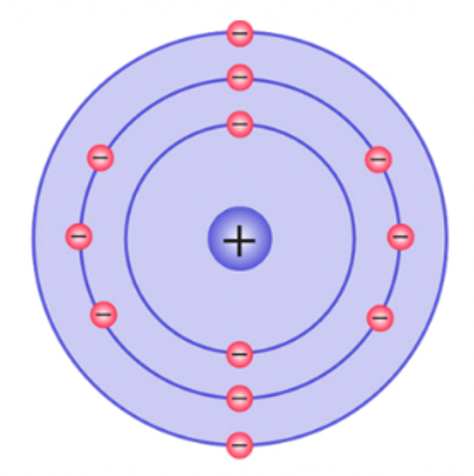
В основу этой модели легли постулаты Бора, которые мы рассмотрим в следующей главе.
Современная нуклонная модель
В 1932 году появилась нуклонная модель Гейзенберга-Иваненко. Модель подразумевает, что в ядре атома находятся не только положительно заряженные протоны, но и нейтральные незаряженные нейтроны.
Нуклоны — частицы, являющиеся составными частями атомного ядра. К нуклонам относятся протоны и нейтроны.
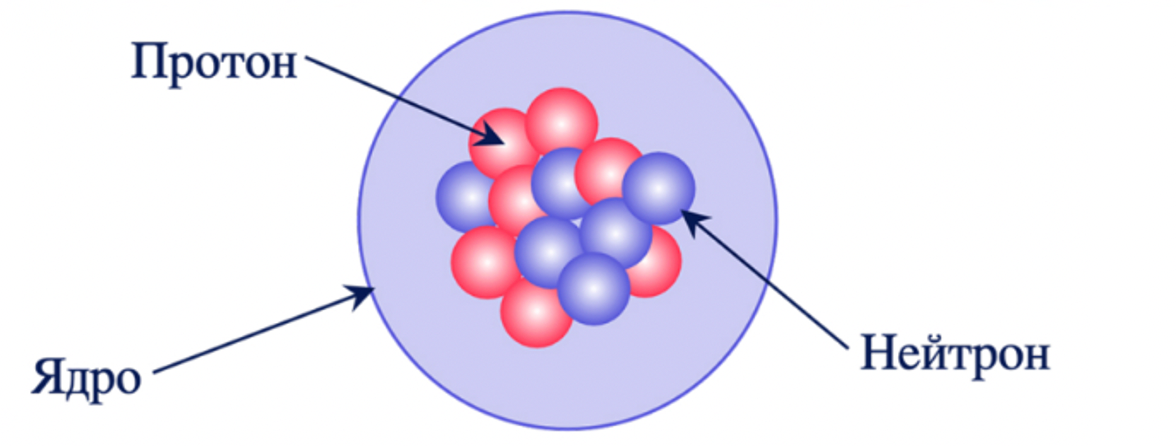
Масса протона составляет $1,673 \cdot 10^{−27}$ кг, а масса нейтрона — $1,675 \cdot 10^{−27}$. Их массы имеют близкие значения, поэтому в некоторых задачах их считают равными.
Масса электрона равна $9,1 \cdot 10^{−31}$ кг, что во много раз меньше, чем масса протона и нейтрона. В связи с этим можно считать, что вся масса атома сосредоточена в ядре, а масса атома примерно равна массе ядра.
Заряд протона равен элементарному заряду, то есть заряду электрона, но взятому со знаком плюс:
$q_p = e = 1,6 \cdot 10^{−19} \text{ Кл}$
Изотопы и таблица Менделеева
Химические свойства элемента определяются только зарядом его ядра (количеством протонов в ядре), количество нейтронов у атома одного и того же элемента может отличаться. Например, в ядре лития всегда находится 3 протона, но количество нейтронов может быть 3 или 4, такие атомы называются изотопами.
Изотопы — атомы, обладающие одинаковым количеством протонов, но разным количеством нейтронов.
Иными словами, изотопы имеют равный заряд ядра, но разную массу.
Одним из примеров изотопов являются изотопы водорода. В нормальном состоянии ядро водорода состоит из 1 протона. Но существуют формы, где в ядро добавляются 1 или 2 нейтрона; они называются дейтерий и тритий, соответственно.
Информация о строении атома содержится в таблице Менделеева и отображается в виде массового и зарядового числа.
Зарядовое число (Z) элемента равно количеству протонов в ядре:
$Z = N_p$
Чтобы найти заряд ядра, нужно умножить зарядовое число на элементарный заряд:
$q_{\text{ядра}} = N_p \cdot e = Z \cdot e$
Массовое число (A) равно сумме количества протонов и нейтронов (нуклонов) в ядре.
$A = N_p + N_n = N_{\text{нуклонов}}$
При расписывании реакций зарядовое число Z элемента X ставят снизу слева, а массовое A − слева сверху.
${}^A_Z X$
В качестве примера рассмотрим атом лития ${}^7_3 Li$.
Количество протонов в ядре равно зарядовому числу − 3. Количество нуклонов равно массовому числу − 7. Количество нейтронов можно найти из формулы $A = N_p + N_n = N_{\text{нуклонов}}$, оно равно разности массового и зарядового числа, то есть 4.
Если атом является электронейтральным, то есть не имеет заряда, то количество протонов совпадает с количеством электронов. Соответственно, число электронов в нейтральном атоме лития равно 3.
Практикум: решение задач
Задание 1
Определите массовое число атома бериллия ${}^9_4 Be$.
Массовое число находится сверху, это число 9.
Ответ: 9.
Задание 2
В опыте рассматриваются электрически нейтральные ядра атомов молибдена ${}^{96}_{42} Mo$ и кальция ${}^{40}_{20} Ca$. Чему равно отношение числа нуклонов в ядре атома молибдена к числу электронов, вращающихся вокруг ядра атома кальция?
Число нуклонов в ядре атома молибдена равно 96 (массовое число), а число электронов, вращающихся вокруг ядра атома кальция, равно 20 (зарядовое число). Так как атом нейтральный, то количество электронов равно количеству протонов в ядре
$\frac{96}{20} = 4,8$.
Ответ: 4,8.
Задание 3
Сколько протонов содержится в ядре атома брома ${}^{80}_{35} Br$?
Количество протонов в ядре равно зарядовому числу, а оно равно 35.
Ответ: 35.
Задание 4
Вокруг ядра электрически нейтрального атома урана вращается 92 электрона. Чему равно число нейтронов в ядрах изотопов урана-234 и урана-235? В ответ запишите только числа, не разделяя их пробелом или другим знаком.
| Число нейтронов в ядре урана-234 | Число нейтронов в ядре урана-235 |
|---|---|
Массовое число урана-234 равно 234, число нейтронов равно разности массового и зарядового числа. 234 − 92 = 142 нейтрона
Аналогично для урана-235, 235 − 92 = 143 нейтрона.
Ответ: 142143.
Задание 5
Опираясь на данные фрагмента периодической системы химических элементов Д. И. Менделеева, представленного на рисунке, определите число нейтронов в ядре самого распространённого изотопа галлия. Нижний индекс массового числа указывает распространённость изотопа в природе (в процентах).
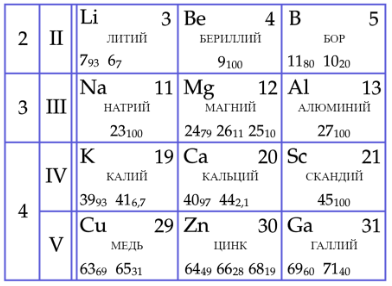
По таблице видим, что галлий с массовым числом 69 встречается в природе в 60% случаев, а с массовым числом 71 — в 40% случаев.
Самый распространённый изотоп галлия — ${}^{69}_{31} Ga$.
$n = A − Z = 69 − 31 = 38.$
Ответ: 38.
Задание 6
В настоящее время известно 3 изотопа неона, являющегося 10-м элементом периодической системы Д. И. Менделеева, при этом массовое число самого лёгкого из них равно 20, а самого тяжёлого — 22. Определите минимальное и максимальное значения возможного количества нейтронов в ядре атома неона. В ответ запишите только числа, не разделяя их пробелом или другим знаком.
| Минимальное количество нейтронов | Максимальное количество нейтронов |
|---|---|
Исходя из условия задачи, нам нужно рассмотреть два изотопа неона:
${}^{20}_{10} Ne$ и ${}^{22}_{10} Ne$.
У первого изотопа 20 − 10 = 10 нейтронов (минимальное количество).
У второго изотопа 22 − 10 = 12 нейтронов (максимальное количество).
Ответ: 1012.
Задание 7
Определите заряд (в единицах элементарного заряда) и массовое число ядра элемента ${}^A_Z X$, образовавшегося в результате ядерной реакции, описываемой уравнением:
${}^{27}_{13} Al + {}^4_2 He \to {}^A_Z X + {}^1_0 n$
В ответ запишите только числа, не разделяя их пробелом или другим знаком.
| Заряд ядра Z | Массовое число ядра A |
|---|---|
${}^{27}_{13} Al + {}^4_2 He \to {}^A_Z X + {}^1_0 n$
Решим уравнение, взяв верхние коэффициенты:
27 + 4 = A + 1
A = 30 (массовое число)
Решим уравнение, взяв нижние коэффициенты:
13 + 2 = Z + 0
Z = 15 (зарядовое число).
Ответ: 1530.
Авторы:
Саня Эбонит, преподаватель «100балльного репетитора» по физике ЕГЭ;
Кир Синюткин, методист «100балльного репетитора» по физике ЕГЭ