Понятие теплового равновесия
Тепловое равновесие — это состояние изолированной системы тел, при котором между ними не происходит теплообмена.
Что это означает? Представим, что человек берёт стакан с водой температурой 25 °C. Температура тела человека — 36,6 °C. Как только человек возьмёт стакан, тепловое равновесие нарушится: рука начнёт охлаждаться, а вода — нагреваться. Через некоторое время температура воды повысится и сравняется с температурой руки. После этого установится тепловое равновесие.
Внутренняя энергия вещества
Внутренняя энергия (U) — это сумма кинетической и потенциальной энергий молекул вещества.
При переходе вещества из одного агрегатного состояния в другое кинетическая энергия молекул не изменяется, так как температура остаётся постоянной. Однако потенциальная энергия изменяется, поскольку при фазовых переходах меняется расстояние между молекулами.
В модели идеального газа потенциальной энергией взаимодействия молекул пренебрегают, поэтому его внутренняя энергия равна сумме кинетических энергий молекул.

Агрегатные состояния
Агрегатное состояние — это физическое состояние вещества, которое определяется температурой и давлением.
В программу ЕГЭ включены три агрегатных состояния:
- твёрдое,
- жидкое,
- газообразное.

Количество теплоты
Чтобы изменить температуру тела, необходимо передать ему теплоту или отвести её.
Количество теплоты, необходимое для нагревания или охлаждения тела, вычисляется по формуле:
$Q = cm\Delta t$
Где:
Q — количество теплоты, измеряется в джоулях [Дж];
c — удельная теплоёмкость вещества, измеряется в $\frac{\text{Дж}}{\text{кг} \cdot \text{К}}$ или $\frac{\text{Дж}}{\text{кг} \cdot ^\circ C}$;
m — масса вещества, измеряется в кг;
∆t — изменение температуры вещества, измеряется в кельвинах или в градусах Цельсия, так как изменение температуры будет одним и тем же:
∆t = 100 °C − 20 °C = 80 °C
∆T = 373 К − 293 К = 80 К
То есть:
∆t = ∆T
Чем больше удельная теплоёмкость вещества, тем больше нужно теплоты, чтобы нагреть его.
Например, удельная теплоёмкость воды равна $c_{\text{в}} = 4200 \frac{\text{Дж}}{\text{кг} \cdot \text{К}}$, следовательно, чтобы нагреть 1 кг воды на 1 К, необходимо передать воде количество теплоты, равное 4200 Дж.
Удельная теплоёмкость вещества может отличаться в разных агрегатных состояниях, например, удельная теплоёмкость льда равна $c_{\text{л}} = 2100 \frac{\text{Дж}}{\text{кг} \cdot \text{К}}$.
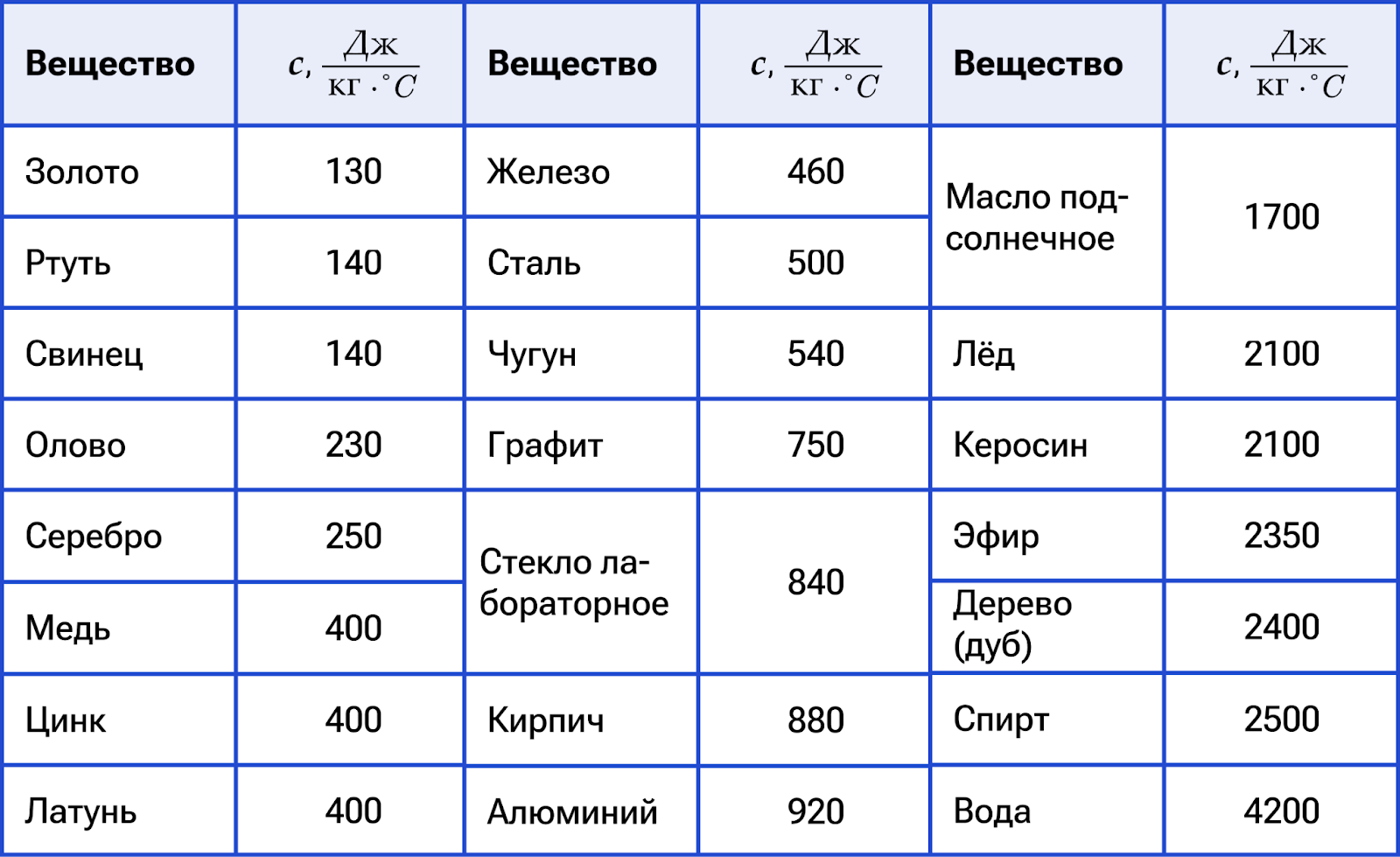
В таблице представлены удельные теплоёмкости основных веществ:
Графики нагревания и охлаждения
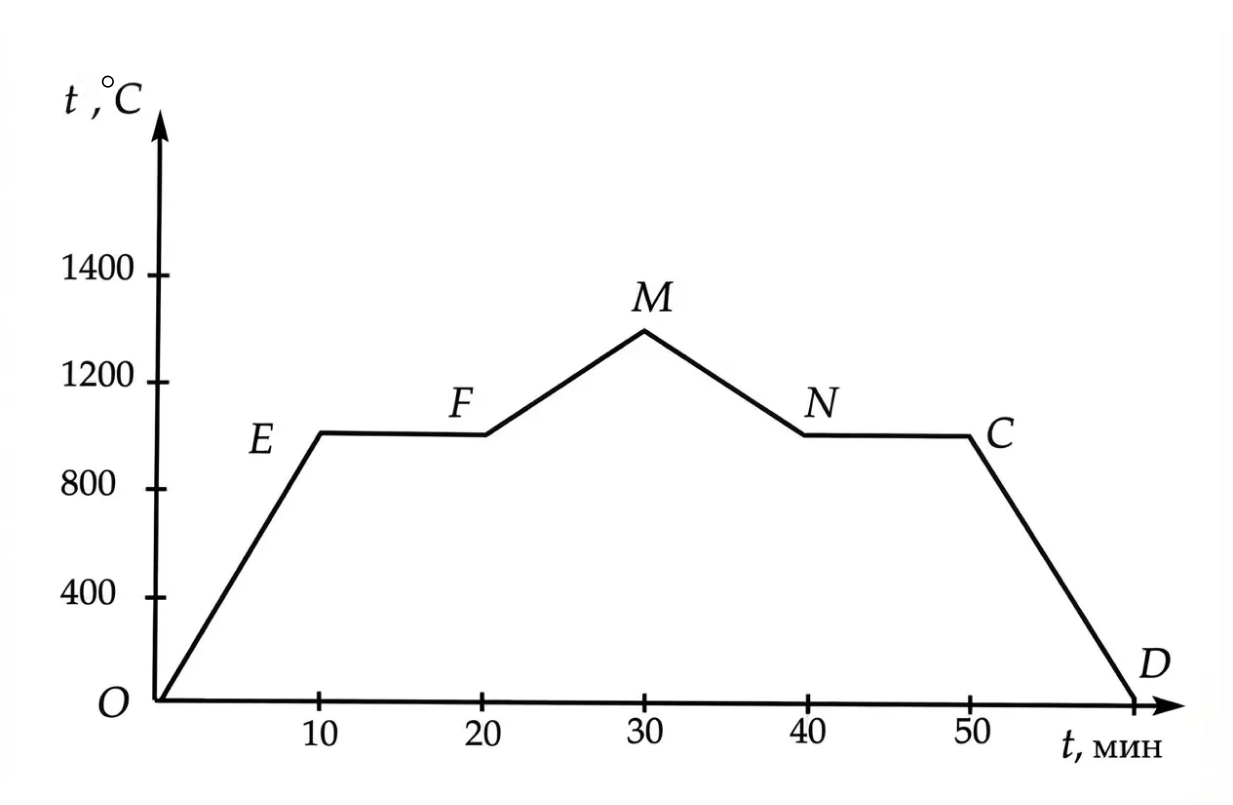
Для решения задач на ЕГЭ очень важно уметь определять процессы по графику зависимости температуры от времени. Процессы нагревания и охлаждения всегда идут под наклоном.
Например, на рисунке ниже процессы OE и FM — нагревание, а процессы MN и CD — охлаждение.
Примеры решения задач
Задание 1
Определи массу медной сковороды, если при охлаждении на 10 ℃ она теряет 1,52 кДж теплоты. Ответ дай в граммах.
Дано:
∆t = 10℃
Q = 1520 Дж
m — ?
Запишем формулу теплоты:
Q = cm∆t
$m = \frac{Q}{c\Delta t} = \frac{1520}{380*10} = 0{,}4 \text{ кг} = 400 \text{ г}$
Ответ: 400 г.
Задание 2
На рисунке приведён график зависимости температуры твёрдого тела от полученного им количества теплоты. Какое количество теплоты получит тело при увеличении его температуры на 90 К? Ответ дай в кДж.
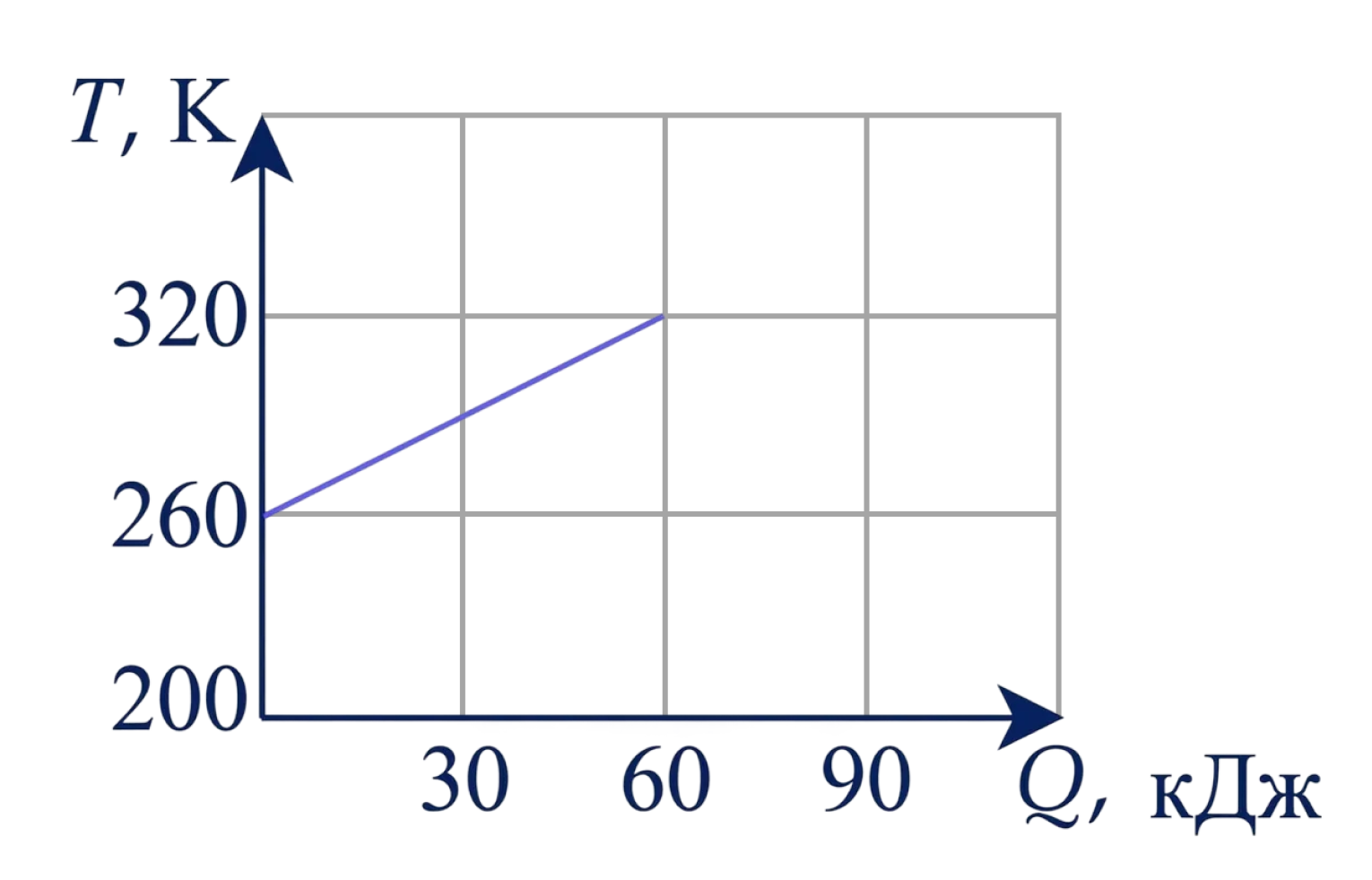
По графику, ∆T₁ = 60 К, Q = 60 кДж
Q₁ = cm∆T₁
Q₂ = cm∆T₂
Поделим одно уравнение на другое, получим:
$\frac{Q_2}{Q_1} = \frac{cm\Delta T_2}{cm\Delta T_1} = \frac{\Delta T_2}{\Delta T_1} = \frac{90}{60} = 1{,}5$
Q₂ = 1,5Q₁ = 1,5 * 60 = 90 кДж
Ответ: 90 кДж.
Авторы:
Саня Эбонит, преподаватель «100балльного репетитора» по физике ЕГЭ;
Кир Синюткин, методист «100балльного репетитора» по физике ЕГЭ